Lawrensium
unsur kimia dengan lambang Lr dan nomor atom 103
(Dialihkan dari Lr (unsur kimia))
Lawrensium (pengucapan: /ləˈrɛnsiəm/) adalah unsur kimia yang berlambang Lr (sebelumnya Lw) dan memiliki nomor atom 103. Unsur ini merupakan unsur sintetik yang radioaktif. Isotop Lawrensium yang paling stabil adalah 266Lr.
103Lr Lawrensium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
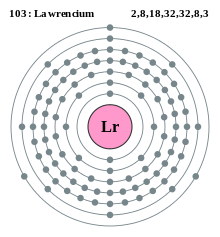 Konfigurasi elektron lawrensium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /lawrènsium/[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | keperakan (diprediksi)[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lawrensium dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 103 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok-d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | aktinida, kadang dianggap sebagai logam transisi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor massa | [266] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Rn] 7s2 5f14 7p1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 32, 32, 8, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 1900 K (1627 °C, 2961 °F) (diprediksi) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 14,4 g/cm3 (diprediksi)[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | +3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,3 (diprediksi)[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 478,6 kJ/mol[5] ke-2: 1428,0 kJ/mol (diprediksi) ke-3: 2219,1 kJ/mol (diprediksi) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | sintetis | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | susunan padat heksagon (hcp) (diprediksi)[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 22537-19-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penamaan | dari E. Lawrence | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penemuan | Laboratorium Nasional Lawrence Berkeley dan Joint Institute for Nuclear Research (1961–1971) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotop lawrensium yang utama | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||

Referensi
sunting- ^ (Indonesia) "Lawrensium". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Emsley, John (2011). Nature's Building Blocks: An A-Z Guide to the Elements (edisi ke-New). New York, NY: Oxford University Press. hlm. 278–279. ISBN 978-0-19-960563-7.
- ^ Gyanchandani, Jyoti; Sikka, S. K. (10 Mei 2011). "Physical properties of the 6 d -series elements from density functional theory: Close similarity to lighter transition metals". Physical Review B. 83 (17): 172101. Bibcode:2011PhRvB..83q2101G. doi:10.1103/PhysRevB.83.172101.
- ^ Brown, Geoffrey (2012). The Inaccessible Earth: An integrated view to its structure and composition. Springer Science & Business Media. hlm. 88. ISBN 9789401115162.
- ^ http://cen.acs.org/articles/93/i15/Lawrencium-Ionization-Energy-Measured.html?cq_ck=1428631698138
- ^ Östlin, A.; Vitos, L. (2011). "First-principles calculation of the structural stability of 6d transition metals". Physical Review B. 84 (11): 113104. Bibcode:2011PhRvB..84k3104O. doi:10.1103/PhysRevB.84.113104.
- ^ http://flerovlab.jinr.ru/she-factory-first-experiment/
Pranala luar
suntingWikimedia Commons memiliki media mengenai Lawrencium.
Lihat entri lawrencium di kamus bebas Wiktionary.
