Tubokurarin klorida
Tubokurarin klorida (juga dikenal dengan d-tubokurarin atau DTC) adalah alkaloid benzilisokuinolina yang secara historis dikenal karena penggunaannya sebagai racun panah. Pada pertengahan tahun 1900-an, obat ini digunakan bersama dengan anestesi untuk memberikan relaksasi otot lurik selama pembedahan atau ventilasi mekanis. Alternatif yang lebih aman, seperti sisatrakurium dan rokuronium bromida, telah banyak menggantikannya sebagai tambahan untuk anestesi klinis dan sekarang jarang digunakan.
| |
|---|---|

| |
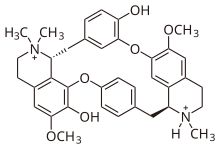
| Nama sistematis (IUPAC) | |
| 6,6′-dimetoksi-2,2′,2′-trimetiltubokuraran-2,2′-diium-7′,12′-diol | |
| Data klinis | |
| AHFS/Drugs.com | International Drug Names |
| MedlinePlus | a682860 |
| Kat. kehamilan | C(AU) |
| Status hukum | ℞ Preskripsi saja |
| Rute | IV |
| Data farmakokinetik | |
| Bioavailabilitas | 100% (IV) |
| Ikatan protein | 50% |
| Waktu paruh | 1–2 jam |
| Pengenal | |
| Nomor CAS | 6989-98-6 |
| Kode ATC | M03AA02 |
| PubChem | CID 6000 |
| Ligan IUPHAR | 2294 |
| DrugBank | DB01199 |
| ChemSpider | 5778 |
| UNII | 900961Z8VR |
| ChEBI | CHEBI:9774 |
| ChEMBL | CHEMBL1687 |
| Data kimia | |
| Rumus | C37H42Cl2N2O6 |
| SMILES | eMolecules & PubChem |
| |
Sejarah
suntingTubokurarin adalah alkaloid monokuartener alami yang diperoleh dari kulit tumbuhan Menispermaceae Amerika Selatan, Chondrodendron tomentosum, tumbuhan merambat yang dikenal di dunia Eropa sejak penaklukan Spanyol di Amerika Selatan. Curare telah digunakan sebagai sumber racun panah oleh penduduk asli Amerika Selatan untuk berburu binatang, dan mereka dapat memakan daging binatang yang terkontaminasi tanpa efek samping karena tubokurarin tidak dapat dengan mudah melewati membran mukosa. Dengan demikian, tubokurarin hanya efektif jika diberikan secara parenteral, seperti yang ditunjukkan oleh Claude Bernard, yang juga menunjukkan bahwa tempat kerjanya berada di persimpangan neuromuskular.[1] Virchow dan Munter mengonfirmasi bahwa tindakan melumpuhkan terbatas pada otot-otot sukarela.[2]
Etimologi
suntingKata curare berasal dari kata dalam bahasa Karibia.[3] Tubokurarin disebut demikian karena beberapa ekstrak tumbuhan yang disebut curare disimpan, dan kemudian dikirim ke Eropa dalam tabung bambu. Demikian pula, curare yang disimpan dalam wadah labu air disebut "labu air curare", meskipun ini biasanya bukan ekstrak dari Chondrodendron, tetapi dari spesies Strychnos, S. toxifera, yang mengandung alkaloid yang berbeda, yaitu toksiferin. Pot curare umumnya merupakan campuran ekstrak dari berbagai genus dalam famili Menispermaceae dan Strychnaceae. Klasifikasi tripartit menjadi curare "tabung", "labu air", dan "pot" awalnya tidak dapat dipertahankan, karena ketidakkonsistenan dalam penggunaan berbagai jenis wadah dan kompleksitas resep racun panah itu sendiri.[4]
Kegunaan
suntingPenggunaan dalam anestesi
suntingGriffith dan Johnson dianggap sebagai pelopor pengenalan klinis formal tubokurarin sebagai tambahan untuk praktik anestesi pada tanggal 23 Januari 1942, di Rumah Sakit Homeopati Montreal.[5] Dalam pengertian ini, tubokurarin adalah agen non-depolarisasi neuromuskular tambahan prototipe. Namun, yang lain sebelum Griffith dan Johnson telah mencoba penggunaan tubokurarin dalam beberapa situasi:[6][7][8] beberapa di bawah kondisi studi yang terkendali,[9][10] sementara yang lain tidak sepenuhnya terkendali dan tetap tidak dipublikasikan.[11] Terlepas dari itu, secara keseluruhan sekitar 30.000 pasien telah diberikan tubokurarin pada tahun 1941, meskipun publikasi Griffith dan Johnson tahun 1942[5] yang memberikan dorongan untuk penggunaan standar agen pemblokiran neuromuskular dalam praktik anestesi klinis – sebuah revolusi yang dengan cepat bermetamorfosis menjadi praktik standar anestesi "seimbang": tiga serangkai hipnosis barbiturat, anestesi inhalasi ringan, dan relaksasi otot.[12] Teknik seperti yang dijelaskan oleh Gray dan Halton dikenal luas sebagai "teknik Liverpool",[12] dan menjadi teknik anestesi standar di Inggris pada tahun 1950-an dan 1960-an untuk pasien dari segala usia dan status fisik. Praktik anestesi klinis masa kini masih menggunakan prinsip utama anestesi seimbang, meskipun dengan beberapa perbedaan untuk mengakomodasi kemajuan teknologi selanjutnya serta diperkenalkannya anestesi gas yang baru dan lebih baik, agen hipnotik dan penghambat neuromuskular, serta intubasi trakea, serta teknik pemantauan yang tidak ada pada masa Gray dan Halton: oksimetri nadi, kapnografi, stimulasi saraf tepi, pemantauan tekanan darah noninvasif, dll.
Sifat kimia
suntingSecara struktural, tubokurarin merupakan turunan benzilisokuinolin. Strukturnya, ketika pertama kali dijelaskan pada tahun 1948 dan selama bertahun-tahun,[13] secara keliru dianggap sebagai bis-kuartener: dengan kata lain, ia dianggap sebagai alkaloid N,N-dimetilasi. Pada tahun 1970, struktur yang benar akhirnya ditetapkan,[14] yang menunjukkan salah satu dari dua nitrogen tersebut bersifat tersier, yang sebenarnya merupakan alkaloid mono-N-metilasi.
Biosintesis
suntingBiosintesis tubokurarin melibatkan penggabungan radikal dari dua enantiomer N-metilkoklaurin. (R) dan (S)-N-metilkoklaurin berasal dari reaksi mirip Mannich antara dopamin dan 4-hidroksifenilasetaldehida, yang difasilitasi oleh norkoklaurin sintase (NCS). Baik dopamin maupun 4-hidroksifenilasetaldehida berasal dari L-tirosina. Metilasi substituen amina dan hidroksil difasilitasi oleh S-adenosil metionina (SAM). Satu gugus metil hadir pada setiap atom nitrogen sebelum penggabungan radikal. Gugus metil tambahan ditransfer untuk membentuk tubokurarin, dengan satu gugus N,N-dimetilamino kuartener.[15]
Efek biologis
suntingTanpa intervensi, asetilkolina (ACh) di sistem saraf tepi mengaktifkan otot rangka. Asetilkolin diproduksi di badan neuron oleh kolina asetiltransferase dan diangkut ke akson menuju celah sinaptik. Tubokurarin klorida bertindak sebagai antagonis untuk reseptor asetilkolin nikotinik (nAChr), yang berarti ia memblokir situs reseptor dari ACh.[17] Hal ini mungkin disebabkan oleh motif struktur amino kuartener yang ditemukan pada kedua molekul tersebut.
Farmakologi klinis
suntingUnna dkk. melaporkan efek tubokurarin pada manusia:
Empat puluh lima detik setelah dimulainya penyuntikan, kelopak mata terasa berat dan diplopia sementara. Setelah penyuntikan selesai, diplopia menjadi tetap, tetapi hanya dapat diperhatikan ketika kelopak mata subjek diangkat oleh operator. Saat kurarisasi berlangsung, subjek merasakan seolah-olah otot-otot wajah, otot-otot lidah, faring, rahang bawah, otot-otot leher dan punggung, serta otot-otot ekstremitas menjadi rileks dalam urutan tersebut. Bersamaan dengan kelumpuhan faring dan otot-otot rahang, subjek juga mengalami ketidakmampuan untuk menelan ... Tak lama setelah penyuntikan selesai, subjek merasakan sensasi kesulitan bernapas yang meningkat, seolah-olah diperlukan upaya ekstra untuk mempertahankan pertukaran pernapasan yang memadai. Sensasi ini muncul meskipun tidak ada bukti objektif gangguan oksigenasi atau retensi karbon dioksida. Sensasi ini mencapai puncaknya sekitar lima menit setelah penyuntikan, bertepatan dengan penurunan maksimum kapasitas vital. Pada sebagian besar percobaan, laju pernapasan meningkat sekitar 50–100 persen pada menit-menit pertama setelah penyuntikan salah satu obat sementara volume tidal menurun.[18]
Tubokurarin memiliki waktu mulai sekitar 5 menit yang relatif lambat di antara obat-obatan penghambat neuromuskular, dan memiliki durasi kerja 60 hingga 120 menit.[19][20] Obat ini juga menyebabkan pelepasan histamin,[21] yang sekarang menjadi ciri khas yang dikenal dari golongan tetrahidroisiokuinolinium dari agen penghambat neuromuskular. Pelepasan histamin dikaitkan dengan bronkospasme, hipotensi, dan sekresi saliva, sehingga berbahaya bagi penderita asma, anak-anak, dan mereka yang sedang hamil atau menyusui.[22] Namun, kerugian utama dalam penggunaan tubokurarin adalah efek penghambatan ganglionnya yang signifikan,[23] yang bermanifestasi sebagai hipotensi,[24] pada banyak pasien; hal ini merupakan kontraindikasi relatif terhadap penggunaannya pada pasien dengan iskemia miokard.
Karena kekurangan tubocurare, banyak upaya penelitian dilakukan segera setelah diperkenalkan secara klinis untuk menemukan pengganti yang sesuai. Upaya tersebut menghasilkan banyak senyawa yang berasal dari hubungan struktur-aktivitas yang dikembangkan dari molekul tubocurare. Beberapa senyawa utama yang telah digunakan secara klinis diidentifikasi dalam kotak templat pelemas otot di bawah ini. Dari sekian banyak yang dicoba sebagai pengganti, hanya sedikit yang sepopuler tubokurarin: pankuronium bromida, vekuronium bromida, rokuronium bromida, atrakurium, dan sisatrakurium. Suksinilkolina adalah obat pelemas otot yang banyak digunakan yang bekerja dengan mengaktifkan, alih-alih memblokir, reseptor ACh.
Penghalang saluran kalium tetraetilamonium (TEA) telah terbukti membalikkan efek tubokurarin. Obat ini dianggap melakukannya dengan meningkatkan pelepasan ACh, yang menangkal efek antagonis tubokurarin pada reseptor ACh.
Penggunaan sebagai pengobatan gigitan laba-laba
suntingLaba-laba dari genus Latrodectus memiliki α-latrotoksin dalam bisanya. Laba-laba yang paling terkenal dalam genus ini adalah laba-laba janda hitam. α-latrotoksin menyebabkan pelepasan neurotransmiter ke celah sinaptik, termasuk asetilkolin.[25] Gigitan biasanya tidak berakibat fatal, tetapi menyebabkan rasa sakit yang signifikan selain kejang otot. Bisanya adalah yang paling merusak ujung saraf, tetapi pemberian d-tubokurarin klorida memblokir nAChr, mengurangi rasa sakit dan kejang otot, sementara antibisa dapat diberikan.[26]
Toksikologi
suntingSeseorang yang diberi tubokurarin klorida tidak akan mampu menggerakkan otot-otot sukarela, termasuk diafragma. Dosis yang cukup besar akan mengakibatkan kematian akibat kegagalan pernapasan kecuali ventilasi buatan dimulai. LD50 untuk tikus dan kelinci masing-masing adalah 0,13 mg/kg dan 0,146 mg/kg secara intravena. Zat ini melepaskan histamin dan menyebabkan hipotensi.[27]
Referensi
sunting- ^ Bernard C (1856). "Analyse physiologie des propriétés des actions de curare et de la nicotine sure systèmes musculaire et nerveux au moyen du curare". Compt. Rend. 43: 305–319.
- ^ Betcher AM (1977). "The civilizing of curare: a history of its development and introduction into anesthesiology". Anesthesia and Analgesia. 56 (2): 305–319. doi:10.1213/00000539-197703000-00032 . PMID 322548.
- ^ "Definition of CURARE". www.merriam-webster.com (dalam bahasa Inggris). Diakses tanggal 2024-11-24.
- ^ The Alkaloids: Chemistry and Physiology ed. R.H.F. Manske (Dominion Rubber Research Laboratory Guelph, Ontario) Academic Press Inc., publishers New York 1955 Volume 5: Pharmacology
- ^ a b Griffith HR, Johnson GE (1942). "The use of curare in general anesthesia". Anesthesiology. 3 (4): 418–420. doi:10.1097/00000542-194207000-00006 .
- ^ Läwen A (1912). "Ueber die verbindung der lokakanaesthesie und epidurale injektion anesthesiernder losungen bei tabischen magenkrisen". Beitr Klin Chir. 80: 168–189.
- ^ Wilkinson DJ (January 1991). "Dr F.P. de Caux--the first user of curare for anesthesia in England". Anaesthesia. 46 (1): 49–51. doi:10.1111/j.1365-2044.1991.tb09317.x . PMID 1996757.
- ^ Bennett AE (1941). "Curare: a preventive of traumatic complications in electroconvulsive shock therapy". Am J Psychiatry. 97: 1040–1060. doi:10.1176/ajp.97.5.1040.
- ^ West R (October 1984). "An excursion into pharmacology: curare in medicine". Medical History. 28 (4): 391–405. doi:10.1017/s0025727300036279. PMC 1140012 . PMID 6390032.
- ^ Burman MS (1939). "Therapeutic use of curare and erythroidine hydrochloride for spastic and dystonic states". Arch Neurol Psychiatry. 41 (2): 307–327. doi:10.1001/archneurpsyc.1939.02270140093008.
- ^ Bevan DR (1992). ""Curare". In: Maltby JR, Shephard DAE (Eds.), Harold Griffith – His Life and Legacy". Can J Anaesth. 39 (1): 49–55.
- ^ a b Gray TC, Halton J (August 1946). "Curarine with Balanced Anaesthesia". British Medical Journal. 2 (4469): 293–295. doi:10.1136/bmj.2.4469.293. PMC 2054113 . PMID 20786887.
- ^ King H (1948). "64. Curare alkaloids. Part VII. Constitution of dextrotubocurarine chloride". J Chem Soc: 265. doi:10.1039/jr9480000265.
- ^ Everett AJ, Lowe LA, Wilkinson S (1970). "Revision of the structures of (+)-tubocurarine chloride and (+)-chondrocurine". J. Chem. Soc. Chem. Commun. (16): 1020. doi:10.1039/c29700001020.
- ^ Dewick, P. M. Medicinal Natural Products; a Biosynthetic Approach. 3rd ed.; John Wiley and Sons Ltd.: 2009.
- ^ Katzung BG (2001). Basic and clinical pharmacology:Introduction to autonomic pharmacology (edisi ke-8). The McGraw Hill Companies. hlm. 75–91. ISBN 978-0-07-160405-5.
- ^ Wenningmann I, Dilger JP (October 2001). "The kinetics of inhibition of nicotinic acetylcholine receptors by (+)-tubocurarine and pancuronium". Molecular Pharmacology. 60 (4): 790–796. PMID 11562442.
- ^ Unna KR (March 1950). "Evaluation Of Curarizing Drugs in Man". The Journal of Pharmacology and Experimental Therapeutics. 98.
- ^ Thompson MA (February 1980). "Muscle relaxant drugs". British Journal of Hospital Medicine. 23 (2): 153–4, 163–4, 167–8 passim. PMID 6102875.
- ^ Page 151 in: Rang HP (2003). Pharmacology. Edinburgh: Churchill Livingstone. ISBN 0-443-07145-4. OCLC 51622037.
- ^ Maclagen J (1976). "Competitive Neuromuscular Blocking Drugs". Dalam Zaimis E. Neuromuscular Junction. Handbook of Experimental Pharmacology. 42. Berlin: Springer-Verlag. hlm. 421–486. doi:10.1007/978-3-642-45476-9_6. ISBN 978-3-642-45476-9.
- ^ "d-Tubocurarine (Prototype Nondepolarizing Neuromuscular Blocker)". Tulane University. Diakses tanggal 4 May 2015.
- ^ Bowman WC, Webb SN (October 1972). "Neuromuscular blocking and ganglion blocking activities of some acetylcholine antagonists in the cat". The Journal of Pharmacy and Pharmacology. 24 (10): 762–772. doi:10.1111/j.2042-7158.1972.tb08880.x. PMID 4403972.
- ^ Coleman AJ, Downing JW, Leary WP, Moyes DG, Styles M (October 1972). "The immediate cardiovascular effects of pancuronium, alcuronium and tubocurarine in man". Anaesthesia. 27 (4): 415–422. doi:10.1111/j.1365-2044.1972.tb08247.x . PMID 4264060.
- ^ Südhof TC (March 2001). "alpha-Latrotoxin and its receptors: neurexins and CIRL/latrophilins". Annual Review of Neuroscience. 24: 933–962. doi:10.1146/annurev.neuro.24.1.933. PMID 11520923.
- ^ Allen GW (September 1953). "Black widow spider (Latrodectus mactans) poisoning treated with d-tubocurarine chloride". Annals of Internal Medicine. 39 (3): 624–625. doi:10.7326/0003-4819-39-3-624. PMID 13080907.
- ^ Gesler RM, Hoppe JO (December 1956). "3, 6-bis(3-diethylaminopropoxy) pyridazine bismethiodide, a long-acting neuromuscular blocking agent". The Journal of Pharmacology and Experimental Therapeutics. 118 (4): 395–406. PMID 13385800.