Leflunomida
Leflunomida adalah obat antirematik pemodifikasi penyakit (DMARD) imunosupresif,[2] yang digunakan pada rheumatoid arthritis sedang hingga berat dan artritis psoriatis. Obat ini merupakan penghambat sintesis pirimidin yang bekerja dengan menghambat dihidroorotat dehidrogenase.[3]
| |
|---|---|

| |
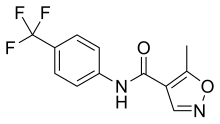
| Nama sistematis (IUPAC) | |
| 5-metil-N-[4-(trifluorometil) fenil]-isoksazola-4-karboksamida | |
| Data klinis | |
| Nama dagang | Arava, Lefumide, Arabloc, dll |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a600032 |
| Data lisensi | EMA:pranala, US Daily Med:pranala |
| Kat. kehamilan | X(AU) |
| Status hukum | Harus dengan resep dokter (S4) (AU) ℞-only (CA) POM (UK) ℞-only (US) |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | 80%[1] |
| Ikatan protein | >99%[1] |
| Metabolisme | mukosa GI dan hati[1] |
| Waktu paruh | 14–18 hari[1] |
| Ekskresi | Feses (48%), urin (43%)[1] |
| Pengenal | |
| Nomor CAS | 75706-12-6 |
| Kode ATC | L04AK01 |
| PubChem | CID 3899 |
| Ligan IUPHAR | 6825 |
| DrugBank | DB01097 |
| ChemSpider | 3762 |
| UNII | G162GK9U4W |
| KEGG | D00749 |
| ChEBI | CHEBI:6402 |
| ChEMBL | CHEMBL960 |
| Data kimia | |
| Rumus | C12H9F3N2O2 |
| |
Kegunaan dalam medis
suntingArtritis reumatoid dan artritis psoriatis merupakan satu-satunya indikasi yang telah menerima persetujuan regulasi.[1][4] Arava dikembangkan oleh Sanofi Aventis dan disetujui oleh Badan Pengawas Obat dan Makanan Amerika Serikat pada tahun 1998. Studi klinis mengenai penyakit-penyakit berikut telah dilakukan:[5] Telah ada laporan mengenai potensi penggunaan kembali leflunomida untuk pengobatan tumor padat dengan kehilangan penekan tumor (PTEN).[6][7] Pada tumor PTEN negatif, leflunomida menyebabkan kematian sintetis yang mungkin disebabkan oleh peningkatan permintaan pirimidin pada sel-sel yang tumbuh lebih cepat ini.[7]
- Nefropati virus Polioma BK[8]
- Penyakit Kimura[9]
- Lupus eritematosus sistemik[10]
- Sindrom Felty[11]
- Arteritis Takayasu[12]
- Granulomatosis Wegener[11]
- Ankilosing spodilitis[13]
- Penyakit Crohn[14][15]
- Sarkoidosis[16]
- Uveitis[17]
- Penyakit Still[18]
- Kanker prostat[19]
- Pemfigoid[20]
- Pencegahan penolakan transplantasi organ[21]
- Kehamilan, wanita usia subur (kecuali menggunakan alat kontrasepsi)
- Penyakit hati, hepatitis B/C seropositif
- Infeksi serius yang aktif
- Hipersensitivitas
Efek samping
suntingEfek samping yang membatasi dosis adalah kerusakan hati, penyakit paru-paru, dan imunosupresi.[21] Efek samping yang paling umum (terjadi pada >1% pengonsumsi) adalah (dalam urutan frekuensi yang menurun):[22][23][24][1][4][25][26] diare, infeksi saluran pernapasan, rambut rontok, tekanan darah tinggi, ruam, mual, bronkitis, sakit kepala, sakit perut, tes fungsi hati yang tidak normal, sakit punggung, dispepsia, infeksi saluran kemih, pusing, infeksi, gangguan sendi, gatal, penurunan berat badan, kehilangan nafsu makan, batuk, gastroenteritis, faringitis, stomatitis, tenosinovitis, muntah, kelemahan, reaksi alergi, nyeri dada, kulit kering, eksim, parestesia, pneumonia, rhinitis, sinovitis, kolelitiasis, dan dispnea. Sedangkan efek samping yang jarang terjadi (terjadi pada 0,1–1% pengonsumsi) meliputi:[4] sembelit, seriawan, stomatitis, gangguan pengecapan, trombositopenia, dan urtikaria. Dalam kasus yang jarang terjadi (pada 0,1% pengonsumsi), obat ini dapat menyebabkan:[4] anafilaksis, angioedema, anemia, agranulositosis, eosinofilia, leukopenia, pansitopenia, vaskulitis, nekrolisis epidermal toksik, sindrom Stevens-Johnson, lupus eritematosus kutan, infeksi berat, penyakit paru interstisial, sirosis, dan gagal hati.
Interaksi
suntingPerawatan imunomodulatori lainnya harus dihindari karena potensi efek imunosupresan aditif, atau dalam kasus imunostimulan seperti echinacea atau astragalus, efek terapeutik berkurang. Demikian pula vaksin hidup (seperti vaksin haemophilus influenzae tipe b dan vaksin demam kuning) harus dihindari karena potensi infeksi parah akibat sifat imunosupresif dari perawatan tersebut.[1]
Penggunaan metotreksat secara bersamaan dapat menyebabkan kerusakan hati atau hepatotoksisitas yang parah atau bahkan fatal. Tujuh puluh lima persen dari semua kasus kerusakan hati parah yang dilaporkan hingga awal tahun 2001 terlihat pada terapi obat gabungan leflunomida plus metotreksat. Namun, beberapa penelitian telah menunjukkan bahwa kombinasi metotreksat dan leflunomida pada pasien dengan artritis reumatoid memberikan hasil yang lebih baik daripada salah satu obat saja.[27]
Farmakologi
suntingMekanisme kerja
suntingLeflunomida adalah obat imunomodulator yang mencapai efeknya dengan menghambat enzim mitokondria dihidroorotat dehidrogenase (DHODH), yang memainkan peran penting dalam sintesis de novo uridina monofosfat (rUMP), yang diperlukan untuk sintesis DNA dan RNA. Oleh karena itu, leflunomida menghambat reproduksi sel yang membelah dengan cepat, terutama limfosit.[21]
Penghambatan DHODH manusia oleh teriflunomida, metabolit aktif leflunomide, terjadi pada kadar (sekitar 600 nM) yang dicapai selama pengobatan artritis reumatoid (RA).[28] Teriflunomida juga menghambat beberapa tirosina kinase.[21] Teriflunomida mencegah perluasan limfosit yang aktif dan autoimun dengan mengganggu perkembangan siklus selnya sementara sel nonlimfoid mampu menggunakan jalur lain untuk membuat ribonukleotidanya, dengan menggunakan jalur pirimidin penyelamatan, yang membuatnya kurang bergantung pada sintesis de novo.[28] Teriflunomida juga memiliki efek antivirus terhadap banyak virus termasuk CMV, HSV1 dan virus BK, yang dicapai dengan menghambat replikasi virus dengan mengganggu tegumentasi nukleokapsid dan dengan demikian perakitan virion.[21]
Farmakokinetik
suntingIa memiliki bioavailabilitas oral sebesar 80%, pengikatan protein >99%, tempat metabolisme mukosa GI dan hati, volume distribusi (Vd) sebesar 0,13 L/kg, waktu paruh eliminasi 14–18 hari dan rute ekskresi feses (48%) dan urin (43%).[22][1][21]
Metabolisme leflunomida
suntingTeriflunomida adalah metabolit aktif utama leflunomida in vivo. Setelah pemberian leflunomida, 70% obat yang diberikan berubah menjadi teriflunomida. Satu-satunya perbedaan antara molekul-molekul tersebut adalah pembukaan cincin isoksazola. Setelah pemberian leflunomida secara oral in vivo, cincin isoksazol leflunomida terbuka dan teriflunomida terbentuk.[29]
"Terlepas dari zat yang diberikan (leflunomida atau teriflunomida), molekulnya sama (teriflunomida); molekul yang memberikan tindakan farmakologis, imunologis, atau metabolik dengan tujuan memulihkan, mengoreksi atau memodifikasi fungsi fisiologis, dan tidak menghadirkan entitas kimia baru kepada pasien dalam penggunaan klinis."[29] Oleh karena itu, Badan Pengawas Obat Eropa (EMA) awalnya tidak menganggap teriflunomida sebagai zat aktif baru.[32]
Referensi
sunting- ^ a b c d e f g h i j "Arava (leflunomide) dosing, indications, interactions, adverse effects, and more". Medscape Reference. WebMD. Diakses tanggal 11 March 2014.
- ^ Dougados M, Emery P, Lemmel EM, Zerbini CA, Brin S, van Riel P (January 2005). "When a DMARD fails, should patients switch to sulfasalazine or add sulfasalazine to continuing leflunomide?". Annals of the Rheumatic Diseases. 64 (1): 44–51. doi:10.1136/ard.2003.016709. PMC 1755199 . PMID 15271770.
- ^ Pinto P, Dougados M (2006). "Leflunomide in clinical practice" (PDF). Acta Reumatologica Portuguesa. 31 (3): 215–24. PMID 17094333.
- ^ a b c d Rossi S, ed. (2013). Australian Medicines Handbook. Adelaide: The Australian Medicines Handbook Unit Trust. ISBN 978-0-9805790-9-3.[halaman dibutuhkan]
- ^ "Leflunomide Search". ClinicalTrials.gov. U.S. National Library of Medicine.
- ^ Ozturk S, Mathur D, Zhou RW, Mulholland D, Parsons R (December 2020). "Leflunomide triggers synthetic lethality in PTEN-deficient prostate cancer". Prostate Cancer and Prostatic Diseases. 23 (4): 718–723. doi:10.1038/s41391-020-0251-1. PMC 7666085 . PMID 32661432.
- ^ a b Mathur D, Stratikopoulos E, Ozturk S, Steinbach N, Pegno S, Schoenfeld S, Yong R, Murty VV, Asara JM, Cantley LC, Parsons R (April 2017). "PTEN Regulates Glutamine Flux to Pyrimidine Synthesis and Sensitivity to Dihydroorotate Dehydrogenase Inhibition". Cancer Discovery. 7 (4): 380–390. doi:10.1158/2159-8290.CD-16-0612. PMC 5562025 . PMID 28255082.
- ^ Blanckaert K, De Vriese AS (December 2006). "Current recommendations for diagnosis and management of polyoma BK virus nephropathy in renal transplant recipients". Nephrology, Dialysis, Transplantation. 21 (12): 3364–7. doi:10.1093/ndt/gfl404 . PMID 16998219.
- ^ Dai L, Wei XN, Zheng DH, Mo YQ, Pessler F, Zhang BY (June 2011). "Effective treatment of Kimura's disease with leflunomide in combination with glucocorticoids". Clinical Rheumatology. 30 (6): 859–65. doi:10.1007/s10067-011-1689-2. PMID 21286771.
- ^ Wu GC, Xu XD, Huang Q, Wu H (February 2013). "Leflunomide: friend or foe for systemic lupus erythematosus?". Rheumatology International. 33 (2): 273–6. doi:10.1007/s00296-012-2508-z. PMID 22961090.
- ^ a b Sanders S, Harisdangkul V (April 2002). "Leflunomide for the treatment of rheumatoid arthritis and autoimmunity". The American Journal of the Medical Sciences. 323 (4): 190–3. doi:10.1097/00000441-200204000-00004. PMID 12003373.
- ^ Unizony S, Stone JH, Stone JR (January 2013). "New treatment strategies in large-vessel vasculitis". Current Opinion in Rheumatology. 25 (1): 3–9. doi:10.1097/BOR.0b013e32835b133a . PMID 23114585.
- ^ Haibel H, Rudwaleit M, Braun J, Sieper J (January 2005). "Six months open label trial of leflunomide in active ankylosing spondylitis". Annals of the Rheumatic Diseases. 64 (1): 124–6. doi:10.1136/ard.2003.019174. PMC 1755172 . PMID 15608310.
- ^ Prajapati DN, Knox JF, Emmons J, Saeian K, Csuka ME, Binion DG (August 2003). "Leflunomide treatment of Crohn's disease patients intolerant to standard immunomodulator therapy". Journal of Clinical Gastroenterology. 37 (2): 125–8. doi:10.1097/00004836-200308000-00006. PMID 12869881.
- ^ Holtmann MH, Gerts AL, Weinman A, Galle PR, Neurath MF (April 2008). "Treatment of Crohn's disease with leflunomide as second-line immunosuppression : a phase 1 open-label trial on efficacy, tolerability and safety". Digestive Diseases and Sciences. 53 (4): 1025–32. doi:10.1007/s10620-007-9953-7. PMID 17934840.
- ^ Panselinas E, Judson MA (October 2012). "Acute pulmonary exacerbations of sarcoidosis". Chest. 142 (4): 827–836. doi:10.1378/chest.12-1060 . PMID 23032450.
- ^ Roy M (August 2007). "Early clinical experience with leflunomide in uveitis". Canadian Journal of Ophthalmology. 42 (4): 634. doi:10.3129/can.j.ophthalmol.i07-085. PMID 17641721.
- ^ Pirildar T (May 2003). "Treatment of adult-onset Still's disease with leflunomide and chloroquine combination in two patients". Clinical Rheumatology. 22 (2): 157. doi:10.1007/s10067-002-0667-0. PMID 12740686.
- ^ Nomor uji klinis NCT00004071 for "Mitoxantrone and Prednisone With or Without Leflunomide in Treating Patients With Stage IV Prostate Cancer" di ClinicalTrials.gov
- ^ Nomor uji klinis NCT00802243 for "Leflunomide Associated With Topical Corticosteroids for Bullous Pemphigoid (ARABUL)" di ClinicalTrials.gov
- ^ a b c d e f Teschner S, Burst V (September 2010). "Leflunomide: a drug with a potential beyond rheumatology". Immunotherapy. 2 (5): 637–50. doi:10.2217/imt.10.52. PMID 20874647.
- ^ a b "Arava Product Information" (PDF). TGA eBusiness Services. sanofi-aventis australia pty ltd. 7 August 2012. Diakses tanggal 11 March 2014.
- ^ "Arava 10mg Tablets - Summary of Product Characteristic". electronic Medicines Compendium. Sanofi. 21 February 2014. Diakses tanggal 11 March 2014.
- ^ "Arava (leflunomide) tablet, film coated [sanofi-aventis U.S. LLC]". DailyMed. sanofi-aventis U.S. LLC. November 2012. Diakses tanggal 11 March 2014.
- ^ "Arava : EPAR - Product Information" (PDF). European Medicines Agency. Sanofi-Aventis Deutschland GmbH. 21 November 2013. Diarsipkan dari versi asli (PDF) tanggal 11 March 2014. Diakses tanggal 11 March 2014.
- ^ "Data Sheet Arava" (PDF). Medsafe. sanofi-aventis new zealand limited. 29 June 2012. Diakses tanggal 11 March 2014.
- ^ Lee SS, Park YW, Park JJ, Kang YM, Nam EJ, Kim SI, Lee JH, Yoo WH, Lee SI (2009). "Combination treatment with leflunomide and methotrexate for patients with active rheumatoid arthritis". Scandinavian Journal of Rheumatology. 38 (1): 11–4. doi:10.1080/03009740802360632. PMID 19191187.
- ^ a b Fox RI, Herrmann ML, Frangou CG, Wahl GM, Morris RE, Strand V, Kirschbaum BJ (December 1999). "Mechanism of action for leflunomide in rheumatoid arthritis". Clinical Immunology. 93 (3): 198–208. doi:10.1006/clim.1999.4777. PMID 10600330.
- ^ a b Melchiorri D, van Zwieten-Boot B, Maciulaitis R, Vilceanu M, Bruins Slot K, Hudson I, Hemmings R, Enzmann H, Demolis P. "Assessment report. AUBAGIO (international non-proprietary name: teriflunomide). Procedure No. EMEA/H/C/002514/0000" (PDF). European Medicines Agency. hlm. 119. Diarsipkan dari versi asli (PDF) tanggal 17 July 2015. Diakses tanggal 5 June 2015.
- ^ Rozman B (2002). "Clinical pharmacokinetics of leflunomide". Clinical Pharmacokinetics. 41 (6): 421–30. doi:10.2165/00003088-200241060-00003. PMID 12074690.
- ^ "Clinical Pharmacology/Biopharmaceutics Review. Product: ARAVA (leflunomide tablets). Application Number: NDA 20905" (PDF). U.S. Food and Drug Administration. Center for Drug Evaluation and Research. Diakses tanggal 15 April 2016.
- ^ "Summary of Opinion (Initial Authorisation): Aubagio (teriflunomide)" (PDF). European Medicines Agency. Diarsipkan dari versi asli (PDF) tanggal 13 March 2016. Diakses tanggal 15 April 2016.
Bacaan lebih lanjut
sunting- Shankaranarayana S, Barrett C, Kubler P (February 2013). "The safety of leflunomide". Australian Prescriber. 36 (1): 28–32. doi:10.18773/austprescr.2013.010 .