Asam p-toluenasulfonat
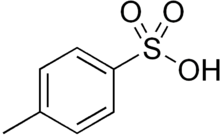
Asam p-toluenasulfonat (PTSA), atau disingkat TsOH, adalah senyawa organik yang memiliki rumus CH3C6H4SO3H. Ia berupa padatan berwarna putih yang larut dalam air, alkohol, dan pelarut organik polar lainnya. Seringkali, TsOH merujuk pada senyawa monohidratnya, TsOH.H2O.
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
asam 4-metilbenzenasulfonat
| |
| Nama lain
asam tosilat
asam p-toluenasulfonat asam tosat PTSA | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Nomor EC | |
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| Sifat | |
| C7H8O3S | |
| Massa molar | 172,20 g/mol 190,22 g/mol (monohidrat) |
| Penampilan | padatan tidak berwarna (putih) |
| Titik lebur | 106-107 °C 103-106 °C (monohidrat) |
| Titik didih | 140 °C pada 20 mmHg |
| 67g/100 ml | |
| Keasaman (pKa) | -2,8 |
| Struktur | |
| tetrahedral pada S | |
| Bahaya | |
| Bahaya utama | iritasi kulit |
| Frasa-R | 36/37/38 |
| Frasa-S | 26 |
| Senyawa terkait | |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
TsOH adalah asam organik yang kuat, satu juta kali lebih kuat daripada asam benzoat. Ia merupakan salah satu asam kuat yang berupa zat padat, sehingga mudah ditimbang. Selain itu, berbeda dengan asam mineral kuat lainnya (terutama asam nitrat, asam sulfat, dan asam perklorat), TsOH bersifat non-oksidator.
Pembuatan dan penanganan
suntingPada skala industri, TsOH dibuat dari sulfonasi toluena. Ia berhidrasi dengan cepat. Umumnya terdapat pula sebagian kecil asam benzenasulfonat dan asam sulfat yang dihasilkan. Ketidakmurnian ini dapat dipisahkan dengan rekristalisasi dari asam klorida, kemudian diikuti dengan pengeringan azeotropik.[2]
TsOH berguna dalam sintesis organik sebagai katalis asam yang larut dalam pelarut organik. Contoh penggunaan asam ini adalah :
Reaksi
suntingAsam p-toluenasulfonat dapat diubah menjadi p-toluenasulfonat anhidrida dengan memanaskannya dengan fosfor pentoksida.[6]
Lihat pula
suntingReferensi
sunting- ^ Merck Index, 11th Edition, 9459.
- ^ Perrin, D. D. and Armarego, W. L. F., Purification of Laboratory Chemicals, Pergamon Press: Oxford, 1988.
- ^ H. Griesser, H.; Öhrlein, R.; Schwab, W.; Ehrler, R.; Jäger, V. (2004). "3-Nitropropanal, 3-Nitropropanol, and 3-Nitropropanal Dimethyl Acetal". Org. Synth.; Coll. Vol. 10: 577.
- ^ Furuta, K. Gao, Q.-z.; Yamamoto, H. (1998). "Chiral (Acyloxy)borane Complex-catalyzed Asymmetric Diels-Alder Reaction: (1R)-1,3,4-Trimethyl-3-cyclohexene-1-carboxaldehyde". Org. Synth.; Coll. Vol. 9: 722.
- ^ Imwinkelried, R.; Schiess, M.; Seebach, D. (1993). "Diisopropyl (2S,3S)-2,3-O-isopropylidenetartrate". Org. Synth.; Coll. Vol. 8: 201.
- ^ L. Field and J. W. McFarland (1963). "p-Toluenesulfonic Anhydride". Org. Synth.; Coll. Vol. 4: 940.