Timbal(II) oksida
Timbal(II) oksida, juga disebut timbal monoksida, adalah senyawa anorganik dengan rumus molekul PbO. PbO terjadi dalam dua polimorf, satu litharge yang memiliki struktur kristal tetragonal dan yang lainnya massicot memiliki kristal struktur kristal ortorombik. Aplikasi modern untuk PbO sebagian besar untuk industri terkemuka berbasis timbal, kaca dan keramik industri, termasuk komponen komputer. Ini adalah oksida amfoter.

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Lead(II) oxide
| |
| Nama lain | |
| Penanda | |
| 3DMet | {{{3DMet}}} |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| Nomor UN | 3288 |
CompTox Dashboard (EPA)
|
|
| Sifat | |
| PbO | |
| Massa molar | 223,20 g/mol |
| Penampilan | Bubuk merah atau kuning |
| Densitas | 9.53 g/cm3 |
| Titik lebur | 888 °C (1.161 K) |
| Titik didih | 1.477 °C (1.750 K) |
| 0,017 g/L[1] | |
| Kelarutan | tidak larut dalam basa encer, alkohol larut dalam basa pekat larut dalam HCl, amonium klorida |
| −42,0·10−6 cm3/mol | |
| Struktur | |
| tetragonal, tP4 | |
| P4/nmm, No. 129 | |
| Bahaya | |
| Lembar data keselamatan | ICSC 0288 |
Klasifikasi UE (DSD) (usang)
|
Repr. Cat. 1/3 Berbahaya (Xn) Berbahaya bagi lingkungan (N) |
| Frasa-R | R61, R20/22, R33, R62, R50/53 |
| Frasa-S | S53, S45, S60, S61 |
| Titik nyala | Tidak mudah terbakar |
| Dosis atau konsentrasi letal (LD, LC): | |
LDLo (terendah tercatat)
|
1400 mg/kg (anjing, oral)[2] |
| Senyawa terkait | |
Anion lain
|
Timbal sulfida Timbal selenida Timbal telurida |
Kation lainnya
|
Karbon monoksida Silikon monoksida Timah(II) oksida |
| Timbal(II,II,IV) oksida Timbal dioksida | |
Senyawa terkait
|
Talium(III) oksida Bismut(III) oksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Preparasi
suntingPbO dapat dibuat dengan memanaskan logam timbal di udara pada suhu kira-kira 600 °C. Pada suhu ini PbO juga merupakan produk akhir dari oksidasi oksida timbal lainnya di udara:[3]
- PbO –(293 °C)→ Pb –(351 °C)→ Pb –(375 °C)→ Pb –(605 °C)→ PbO
Dekomposisi thermal timbal(II) nitrat atau timbal karbonat juga menghasilkan PbO:
- 2 Pb(NO''"; → 2 PbO + 4 NO + O
- PbCO → PbO + CO
PbO diproduksi dalam skala besar sebagai produk antara dalam pengolahan bijih timbal menjadi logam timbal. Bijih timbal yang umum adalah galena (timbal(II) sulfida). Pada suhu tinggi (1000 °C) sulfida diubah menjadi oksida:[4]
- 2 PbS + 3 O2 → 2 PbO + 2 SO2
Timbal logam diperoleh dengan mereduksi PbO dengan karbon monoksida sekitar 1200 °C:[5]
- PbO + CO → Pb + CO2
Struktur
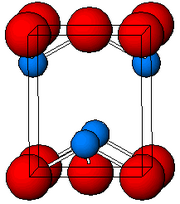
suntingSeperti yang ditentukan oleh kristalografi sinar-X, kedua polimorf, tetragonal dan ortorombik menampilkan piramida empat koordinasi dengan pusat Pb. Dalam bentuk tetragonal keempat ikatan Pb-O memiliki panjang yang sama, tetapi pada ortorombik dua lebih pendek dan dua lebih panjang. Sifat piramida menunjukkan adanya pasangan elektron sunyi yang aktif secara stereo kimia.[6] Bila PbO terjadi pada struktur kisi tetragonal maka disebut litharge; dan jika PbO memiliki struktur kisi ortorombik disebut massicot. PbO dapat diubah dari massicot menjadi litharge atau sebaliknya dengan pemanasan dan pendinginan terkendali.[n 1] Bentuk tetragonal biasanya berwarna merah atau jingga, sedangkan ortorombik biasanya berwarna kuning atau jingga, tetapi warna bukan indikator struktur yang dapat diandalkan.[7] Bentuk tetragonal dan ortorombik PbO terjadi secara alami sebagai mineral langka.
Reaksi
suntingBentuk merah dan kuning dari bahan ini terkait dengan sedikit perubahan entalpi:
- PbO(merah) → PbO(kuning) ΔH = 1,6 kJ/mol
PbO bersifat amfoter, yang berarti dapat bereaksi baik dengan asam maupun basa. Dengan asam, ia membentuk garam Pb2+ melalui perantara cluster okso seperti [Pb''";. Dengan basa kuat, PbO larut membentuk garam plumbit(II):[8]
- PbO + H + OH → [Pb(OH)''";
Aplikasi
suntingJenis timbal dalam kaca timbal biasanya PbO, dan PbO digunakan secara luas dalam pembuatan kaca. Bergantung pada jenis kacanya, manfaat menggunakan PbO dalam kaca antara lain:
- meningkatkan indeks bias kaca,
- menurunkan viskositas kaca,
- meningkatkan resistivitas listrik kaca, dan
- meningkatkan kemampuan kaca untuk menyerap sinar-X.
Menambahkan PbO ke dalam keramik industri (dan juga kaca) membuat bahan lebih inert secara magnetis maupun elektrik (menaikkan suhu Curie) dan sering digunakan untuk tujuan ini.[9] Secara historis PbO juga digunakan secara ekstensif untuk glasir keramik pada keramik rumah tangga, dan meski masih digunakan, tetapi tidak lagi ekstensif. Aplikasi lain yang kurang mendominasi termasuk vulkanisasi karet serta produksi pigmen dan cat tertentu.[10] PbO digunakan pada kaca tabung sinar katode untuk memblokir emisi sinar-X, tetapi terutama di leher dan corong karena dapat menyebabkan perubahan warna saat digunakan di faceplate. Stronsium oksida lebih disukai untuk faceplate.
Konsumsi timbal, dan juga pengolahan PbO, berkorelasi dengan jumlah mobil karena tetap menjadi komponen kunci baterai timbal-asam (aki) kendaraan bermotor.[11]
Penurunan penggunaan atau penggunaan ceruk
suntingCampuran PbO dengan gliserin menempel pada semen keras yang tahan air dan telah digunakan untuk menempelkan kaca samping dan bawah akuarium, dan juga pernah digunakan untuk menyegel panel kaca pada bingkai jendela. Ia juga komponen cat timbal.
Dalam bentuk serbuk litharge tetragonal, PbO dapat dicampur dengan minyak biji rami dan kemudian dididihkan untuk menghasilkan perekat (sizing) tahan cuaca yang digunakan dalam penyepuhan. Litharge akan memberi warna merah tua yang membuat lembaran emas tampak hangat dan berkilau, sementara minyak biji rami akan menanamkan adesi dan permukaan pengikat yang tahan lama.
PbO digunakan dalam reaksi reaksi kondensasi tertentu dalam sintesis organik.[12]
Masalah kesehatan
suntingTimbal oksida bisa berakibat fatal jika tertelan atau terhirup. Ini dapat menyebabkan iritasi pada kulit, mata, dan saluran pernafasan. Ini mempengaruhi jaringan gusi, sistem saraf pusat, ginjal, darah, dan sistem reproduksi. PbO bisa mengalami bioakumulasi pada tanaman dan mamalia.[13]
Catatan kaki
sunting- ^ Contoh sederhana diberikan pada Anil Kumar De (2007), A Text Book of Inorganic Chemistry, hlm. 383. Contoh yang lebih kompleks ada di "9.4 on lead alkoxides", The Chemistry of Metal Alkoxides, Kluwer Academic Publishers, 2002, hlm. 115.
Referensi
sunting- ^ Blei(II)-oxid. Merck
- ^ "Lead compounds (as Pb)". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ N.N. Greenwood, A. Earnshaw (1997), Chemistry of Elements (edisi ke-2nd), Butterworth-Heinemann
- ^ Abdel-Rehim, A. M. (2006), "Thermal and XRD analysis of Egyptian galena", Journal of Thermal Analysis and Calorimetry, 86 (2): 393–401
- ^ Lead Processing @ Universalium.academic.ru. Alt address: Lead processing @ Enwiki.net Diarsipkan 2017-02-22 di Wayback Machine..
- ^ Wells, A. F. (1984), Structural Inorganic Chemistry (edisi ke-5th), Oxford: Clarendon Press, ISBN 0-19-855370-6
- ^ David John Rowe (1983), Lead manufacturing in Britain, hlm. 16
- ^ Holleman, A. F.; Wiberg, E. (2001), Inorganic Chemistry, San Diego: Academic Press, ISBN 0-12-352651-5
- ^ "Chapter 9, Lead Compounds", Ceramic and Glass Materials: Structure, Properties and Processing, Springer, 2008
- ^ Dodd S. Carr (2002), "Lead Compounds", Ullmann's Encyclopedia of Industrial Chemistry, Weinhiem: Wiley-VCH, doi:10.1002/14356007.a15_249
- ^ Charles A. Sutherland, Edward F. Milner, Robert C. Kerby, Herbert Teindl, Albert Melin, Hermann M. Bolt (2005), "Lead", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a15_193.pub2
- ^ Corson, B. B. (1936). "1,4-Diphenylbutadiene". Org. Synth. 16: 28; Coll. Vol. 2: 229.
- ^ "Lead (II) oxide". International Occupational Safety and Health Information Centre. Diarsipkan dari versi asli tanggal 2011-12-15. Diakses tanggal 2009-06-06.
Pranala luar
sunting- (Inggris) Case Studies in Environmental Medicine - Lead Toxicity
- (Inggris) ToxFAQs: Lead
- (Inggris) National Pollutant Inventory - Lead and Lead Compounds Fact Sheet Diarsipkan 2008-01-11 di Wayback Machine.
- (Inggris) Webelements PbO