Amonium besi(III) sulfat
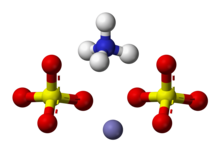
Amonium besi(III) sulfat, NH4Fe(SO4)2·12 H2O, atau NH4[Fe(H2O)6](SO4)2·6 H2O, juga dikenal sebagai feri amonium sulfat (FAS) atau alum besi, merupakan sebuah garam ganda dalam golongan alum, yang terdiri dari senyawa dengan rumus umum AB(SO4)2 · 12 H2O.[2] Ia memiliki penampilan kristal oktahedral berwarna ungu pucat. Terdapat beberapa diskusi mengenai asal usul warna kristal ini, ada yang menganggap warna tersebut berasal dari pengotor dalam senyawa,[3] dan ada pula yang menyatakan bahwa warna tersebut berasal dari kristal itu sendiri.[4]

| |

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Amonium besi(III) sulfat
| |
| Nama lain
Feri amonium sulfat
Alum feri | |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider |
|
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII |
|
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| FeNH4(SO4)2•12H2O | |
| Massa molar | 482,25 g/mol (dodekahidrat) |
| Penampilan | Kristal oktahedral ungu pucat |
| Bau | seperti amonia lemah |
| Densitas | 1,71 g/cm3 |
| Titik lebur | 39 hingga 41 °C (102 hingga 106 °F; 312 hingga 314 K) |
| 1240 g/L | |
| Bahaya | |
| Bahaya utama | Iritan |
| Kategorie:Wikipedia:Gefahrstoffkennzeichnung unbekannt ? | |
| Kategorie:Wikipedia:Gefahrstoffkennzeichnung unbekannt ? | |
| Senyawa terkait | |
Anion lain
|
Amonium besi(III) sitrat Amonium klorida |
Kation lainnya
|
Amonium aluminium sulfat Kalium aluminium sulfat |
Senyawa terkait
|
Amonium besi(II) sulfat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
FAS bersifat paramagnetik,[5] asam dan beracun terhadap mikroorganisme.[6] Ia adalah oksidator lemah, mampu direduksi menjadi garam Mohr, fero amonium sulfat.
Pembuatan
suntingFAS dapat dibuat melalui kristalisasi dari larutan feri sulfat dan amonium sulfat. Besi(II) dalam fero sulfat dioksidasi menjadi feri sulfat dengan penambahan asam sulfat dan nitrat. Setelah penambahan amonium sulfat ke dalam larutan dan redaman dalam larutan, kristal feri amonium sulfat mengendap. Persamaan konversi ini mengabaikan derajat hidrasi dari material yang ada.
Oksidasi: 6 FeSO4 + 2 HNO3 + 3 H2SO4 →3 Fe2(SO4)3 + 2 NO + 4 H2O
Sintesis: Fe2(SO4)3 + (NH4)2SO4 → 2 NH4Fe(SO4)2
Kegunaan
suntingArea penggunaan FAS meliputi pengolahan air limbah,[7] penyamakan kulit,[7] produksi zat warna,[7] dan sebagai bahan etsa dalam produksi komponen elektronik.[8] Ia telah digunakan dalam berbagai aplikasi, meliputi peralatan pendingin adiabatik,[9] analisis biokimia,[10] dan sintesis organik.[11]
Galeri
sunting-
Kristal amonium besi(III) sulfat
-
Kristal amonium besi(III) sulfat setelah 16 hari di udara
Referensi
sunting- ^ "Material Safety Data Sheet. Iron (III) Ammonium Sulfate Dodecahydrate". fscimage.fishersci.com. Diakses tanggal 29 Desember 2023.
- ^ Considine, Douglas M: Chemical and process technology encyclopedia, McGraw-Hill, New York, 1974, hlm. 993
- ^ Christensen, Odin T. "On the Cause of the Amethyst Color of Ferric Alum and of Mixed Crystals of Ferric and Manganic Alum". Chem. Lab. Roy. Vet. Agr. Hochschule, KGL. Danske Vidsk. Selsk. Forh. 1906: 173–95.
- ^ Bonnell, Jane; Philip Perman, Edgar (1921). "CCXXIX.—The colour of iron alum". J. Chem. Soc., Trans. 119: 1994–1997. doi:10.1039/CT9211901994.
- ^ Cooke, Meyer; Wolf (1956). "The Specific Heats of Three Paramagnetic salts at Very Low Temperatures". Proceedings of the Royal Society of London. Series A, Mathematical and Physical Sciences. 237 (1210): 395–403. Bibcode:1956RSPSA.237..395C. doi:10.1098/rspa.1956.0185.
- ^ Wang, Fei; et al. (2008). "Microcalorimetric investigation of the toxic action of ammonium ferric(III)sulfate on the metabolic activity of pure microbes". Environmental Toxicology and Pharmacology. 25 (3): 351–357. doi:10.1016/j.etap.2007.11.004. PMID 21783873.
- ^ a b c Wiley Encyclopedia of inorganic chemistry: Volume 4, hlm. 1704:
- ^ Chen dkk.: United States Patent 5518131 – "Etching molydbenum with ferric sulfate and ferric ammonium sulfate"
- ^ Grant W. Wilson, Peter T. Timbie: "Construction techniques for adiabatic demagnetization refrigerators using ferric ammonium alum". Cryogenics, Volume 39, Nomor 4, (1999), hlm. 319–322
- ^ J. C. Whitehorn: "A system of blood analysis. Supplement II. Simplified method for the determination of chlorides in blood or plasma". Journal of Biological Chemistry (1921), 45 hlm. 449–60.
- ^ Yu, Shanxin; et al. (2005). "Application of ammonium ferric sulfate dodecahydrate in organic synthesis". General Review. 17 (1): 27–30.
| H2SO4 | He | ||||||||||||||||||
| Li2SO4 | BeSO4 | B | Ester ROSO−3 (RO)2SO2 |
(NH4)2SO4 N2H6SO4 (NH3OH)2SO4 |
O | F | Ne | ||||||||||||
| Na2SO4 NaHSO4 |
MgSO4 | Al2(SO4)3 Al2SO4(OAc)4 |
Si | P | SO2−4 | Cl | Ar | ||||||||||||
| K2SO4 KHSO4 |
CaSO4 | Sc2(SO4)3 | Ti(SO4)2 TiOSO4 |
VSO4 V2(SO4)3 VOSO4 |
CrSO4 Cr2(SO4)3 |
MnSO4 Mn2(SO4)3 |
FeSO4 Fe2(SO4)3 |
CoSO4 Co2(SO4)3 |
NiSO4 | CuSO4 Cu2SO4 |
ZnSO4 | Ga2(SO4)3 | Ge | As | Se | Br | Kr | ||
| RbHSO4 Rb2SO4 |
SrSO4 | Y2(SO4)3 | Zr(SO4)2 | Nb | Mo | Tc | Ru | Rh | PdSO4 | Ag2SO4 | CdSO4 | In2(SO4)3 | SnSO4 | Sb2(SO4)3 | Te | I | Xe | ||
| Cs2SO4 | BaSO4 | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg2SO4 HgSO4 |
Tl2SO4 Tl2(SO4)3 |
PbSO4 | Bi2(SO4)3 | Po | At | Rn | |||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| La | Ce2(SO4)3 Ce(SO4)2 |
Pr2(SO4)3 | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb2(SO4)3 | Lu | |||||
| Ac | Th | Pa | U(SO4)2 UO2SO4 |
Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||||