Sel darah merah
Sel darah merah, eritrosit (bahasa Inggris: red blood cell (RBC), erythrocyte)[1] adalah jenis sel darah yang paling banyak dan berfungsi mengikat oksigen yang diperlukan untuk oksidasi jaringan-jaringan tubuh lewat darah dalam hewan bertulang belakang. Terdapat kira-kira 5 juta sel darah merah per mm3. Bagian dalam eritrosit terdiri dari hemoglobin, sebuah biomolekul yang dapat mengikat oksigen. Hemoglobin akan mengambil oksigen dari paru-paru dan insang, dan oksigen akan dilepaskan saat eritrosit melewati pembuluh kapiler. Warna merah sel darah merah sendiri berasal dari warna hemoglobin yang unsur pembuatnya adalah zat besi. Pada manusia, sel darah merah dibuat di sumsum tulang belakang, lalu membentuk kepingan bikonkaf. Di dalam sel darah merah tidak terdapat nukleus. Sel darah merah sendiri aktif selama 120 hari sebelum akhirnya dihancurkan.[2]
| Sel Darah Merah | |
|---|---|
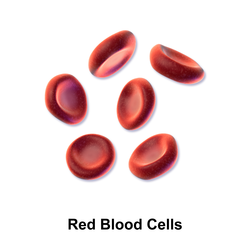 Rendering 3D sel darah merah manusia (ca 6–8 μm in diameter) | |
| Rincian | |
| Fungsi | Oxygen transport |
| Pengidentifikasi | |
| Akronim | RBC |
| MeSH | D004912 |
| TH | H2.00.04.1.01001 |
| FMA | 62845 |
| Daftar istilah mikroanatomi | |
Sel darah merah atau yang juga disebut sebagai eritrosit berasal dari Bahasa Yunani, yaitu erythros berarti merah dan kytos yang berarti selubung/sel)
Eritrosit vertebrata
suntingEritrosit secara umum terdiri dari hemoglobin, sebuah metalloprotein kompleks yang mengandung gugus heme, di mana dalam golongan heme tersebut, atom besi akan tersambung secara temporer dengan molekul oksigen (O2) di paru-paru dan insang, dan kemudian molekul oksigen ini akan di lepas ke seluruh tubuh. Oksigen dapat secara mudah berdifusi lewat membran sel darah merah. Hemoglobin di eritrosit juga membawa beberapa produk buangan seperti CO2 dari jaringan-jaringan di seluruh tubuh. Hampir keseluruhan molekul CO2 tersebut dibawa dalam bentuk bikarbonat dalam plasma darah. Myoglobin, sebuah senyawa yang terkait dengan hemoglobin, berperan sebagai pembawa oksigen di jaringan otot.[3]
Warna dari eritrosit berasal dari gugus heme yang terdapat pada hemoglobin. Sedangkan cairan plasma darah sendiri berwarna kuning kecoklatan, tetapi eritrosit akan berubah warna tergantung pada kondisi hemoglobin. Ketika terikat pada oksigen, eritrosit akan berwarna merah terang dan ketika oksigen dilepas maka warna erirosit akan berwarna lebih gelap, dan akan menimbulkan warna kebiru-biruan pada pembuluh darah dan kulit. Metode tekanan oksimetri mendapat keuntungan dari perubahan warna ini dengan mengukur kejenuhan oksigen pada darah arterial dengan memakai teknik kolorimetri.
Pengurangan jumlah oksigen yang membawa protein di beberapa sel tertentu (daripada larut dalam cairan tubuh) adalah satu tahap penting dalam evolusi makhluk hidup bertulang belakang (vertebrata). Proses ini menyebabkan terbentuknya sel darah merah yang memiliki viskositas rendah, dengan kadar oksigen yang tinggi, dan difusi oksigen yang lebih baik dari sel darah ke jaringan tubuh. Ukuran eritrosit berbeda-beda pada tiap spesies vertebrata. Lebar eritrosit kurang lebih 25% lebih besar daripada diameter pembuluh kapiler dan telah disimpulkan bahwa hal ini meningkatkan pertukaran oksigen dari eritrosit dan jaringan tubuh.[4]
Vertebrata yang diketahui tidak memiliki eritrosit adalah ikan dari familia Channichthyidae. Ikan dari familia Channichtyidae hidup di lingkungan air dingin yang mengandung kadar oksigen yang tinggi dan oksigen secara bebas terlarut dalam darah mereka..[5] Walaupun mereka tidak memakai hemoglobin lagi, sisa-sisa hemoglobin dapat ditemui di genom mereka.[6]
Nukleus
suntingPada mamalia, eritrosit dewasa tidak memiliki nukleus di dalamnya (disebut anukleat), kecuali pada hewan vertebrata non mamalia tertentu seperti salamander dari genus Batrachoseps.[7] Konsentransi asam askorbat di dalam sitoplasma eritrosit anukleat tidak berbeda dengan konsentrasi vitamin C yang terdapat di dalam plasma darah.[8] Hal ini berbeda dengan sel darah yang dilengkapi inti sel atau sel jaringan, sehingga memiliki konsentrasi asam askorbat yang jauh lebih tinggi di dalam sitoplasmanya.
Rendahnya daya tampung eritrosit terhadap asam askorbat disebabkan karena sirnanya transporter SVCT2 ketika eritroblas mulai beranjak dewasa menjadi eritrosit. Meskipun demikian, eritrosit memiliki daya cerap yang tinggi terhadap DHA melalui transporter GLUT1 dan mereduksinya menjadi asam askorbat.
Fungsi lain
suntingKetika eritrosit berada dalam tegangan di pembuluh yang sempit, eritrosit akan melepaskan ATP yang akan menyebabkan dinding jaringan untuk berelaksasi dan melebar.[9]
Eritrosit juga melepaskan senyawa S-nitrosothiol saat hemoglobin terdeoksigenasi, yang juga berfungsi untuk melebarkan pembuluh darah dan melancarkan arus darah supaya darah menuju ke daerah tubuh yang kekurangan oksigen.[10]
Eritrosit juga berperan dalam sistem kekebalan tubuh. Ketika sel darah merah mengalami proses lisis oleh patogen atau bakteri, maka hemoglobin di dalam sel darah merah akan melepaskan radikal bebas yang akan menghancurkan dinding dan membran sel patogen, serta membunuhnya.[11][12]
Eritrosit mamalia
suntingPada awal pembentukannya, eritrosit mamalia memiliki nuklei, tetapi nuklei tersebut akan perlahan-lahan menghilang karena tekanan saat eritrosit menjadi dewasa untuk memberikan ruangan kepada hemoglobin. Namun begitu, kadang tampak lekuk pada sisi tengah eritrosit, di mana dengan itu ia kadang disalah sangkakan sebagai nukleus. Karena alasan ketiadaan nukleus itulah, darah ada pula disebut sebagai eritroplastid, walau nama eritrosit jauh lebih umum.[13] Eritrosit mamalia juga kehilangan organel sel lainnya seperti mitokondria. Maka, eritrosit tidak pernah memakai oksigen yang mereka antarkan, tetapi cenderung menghasilkan pembawa energi ATP lewat proses fermentasi yang diadakan dengan proses glikolisis pada glukosa yang diikuti pembuatan asam laktat. Lebih lanjut lagi bahwa eritrosit tidak memiliki reseptor insulin dan pengambilan glukosa pada eritrosit tidak dikontrol oleh insulin. Karena tidak adanya nuklei dan organel lainnya, eritrosit dewasa tidak mengandung DNA dan tidak dapat mensintesa RNA, dan hal ini membuat eritrosit tidak bisa membelah atau memperbaiki diri mereka sendiri.
Eritrosit mamalia berbentuk kepingan bikonkaf yang diratakan dan diberikan tekanan di bagian tengahnya, dengan bentuk seperti "barbel" jika dilihat secara melintang. Bentuk ini (setelah nuklei dan organelnya dihilangkan) akan mengoptimisasi sel dalam proses pertukaran oksigen dengan jaringan tubuh di sekitarnya. Bentuk sel sangat fleksibel sehingga muat ketika masuk ke dalam pembuluh kapiler yang kecil. Eritrosit biasanya berbentuk bundar, kecuali pada eritrosit di keluarga Camelidae (unta), yang berbentuk oval.
Pada jaringan darah yang besar, eritrosit kadang-kadang muncul dalam tumpukan, tersusun bersampingan. Formasi ini biasa disebut roleaux formation, dan akan muncul lebih banyak ketika tingkat serum protein dinaikkan, seperti contoh ketika peradangan terjadi.
Limpa berperan sebagai waduk eritrosit, tetapi hal ini dibatasi dalam tubuh manusia. Di beberapa hewan mamalia, seperti anjing dan kuda, limpa mengurangi eritrosit dalam jumlah besar, yang akan dibuang pada keadaan bertekanan, di mana proses ini akan menghasilkan kapasitas transpor oksigen yang tinggi.meta
Struktur eritrosit
suntingEritrosit merupakan bagian utama dari sel-sel darah. Setiap mililiter darah mengandung rata-rata sekitar 5 miliar eritrosit (sel darah merah), yang secara klinis sering dilaporkan dalam hitung terdapat 5 juta per milimeter kubik (mm3). Eritrosit berbentuk lempeng bikonkaf,yang merupakan sel gepeng berbentuk piringan yang dibagian tengah dikedua sisinya mencekung,seperti sebuah donat dengan bagian tengah mengepeng bukan berlubang. dengan diameter 8 µm, tepi luar tebalnya 2 µm dan bagian tengah 1 µm.[1]
Sel darah merah memiliki struktur yang jauh lebih sederhana dibandingkan kebanyakan sel pada manusia. Pada hakikatnya, sel darah merah merupakan suatu membran yang membungkus larutan hemoglobin (protein ini membentuk sekitar 95% protein intrasel sel darah merah), dan tidak memiliki organel sel, misalnya mitokondria, lisosom atau aparatus Golgi. Sel darah manusia, seperti sebagian sel darah merah pada hewan, tidak berinti. Namun, sel darah merah tidak inert secara metabolis. Melalui proses glikolisis, sel darah merah membentuk ATP yang berperan penting dalam proses untuk mempertahankan bentuknya yang bikonkaf dan juga dalam pengaturan transpor ion (mis. oleh Na+-K+ ATPase dan protein penukar anion serta pengaturan air keluar-masuk sel. Bentuk bikonkaf ini meningkatkan rasio permukaan-terhadap-volume sel darah merah sehingga mempermudah pertukaran gas. Sel darah merah mengandung komponen sitoskeletal yang berperan penting dalam menentukan bentuknya.[2]
Metabolisme eritrosit
suntingEritrosit adalah cakram bikonkaf yang fleksibel dengan kemampuan menghasilkan energi sebagai adenosin trifosfat (ATP) melalui jalur gikolisis anaerob(Embden Meyerhof) dan menghasilkan kekuatan pereduksi sebagai NADH melalui jalur ini serta sebagai nikotamida adenine dinukleotida fosfat tereduksi (NADPH) melalui jalur pintas heksosa monofosfat (hexsose monophosphate shunt) (Hoffbrand et al, 2005). Jalur Embden-Meyerhof juga menghasilkan NADH yang diperlukan oleh enzim methemoglobin reduktase untuk mereduksi methemoglobin (hemoglobin teroksidasi) yang tidak berfungsi, yang mengandung besi ferri (dihasilkan oleh oksidasi sekitar 3% hemoglobin setiap hari) menjadi hemoglobin tereduksi yang aktif berfungsi. 2,3-DPG yang dihasilkan pada pintas Luebering-Rapoport (Luebering-Rapoport Shunt), atau jalur samping pada jalur ini membentuk suatu kompleks 1:1 dengan hemoglobin, dan seperti telah disebutkan di atas, penting dalam regulasi afinitas hemoglobin terhadap oksigen (Hoffbrand et al, 2005)[14]. Jalur Heksosa Monofosfat (pentosa fosfat). Sekitar 5% glikolisis terjadi melalui jalur oksidatif ini, dengan perubahan glukosa-6-fosfat menjadi 6-fosfo-glukonat dan kemudian menjadi ribulosa-5-fosfat. NADPH dihasilkan dan berkaitan dengan glutation yang mempertahankan gugus sulfhidril (SH) tetap utuh dalam sel, termasuk SH dalam hemoglobin dan membran eritrosit. NADPH juga digunakan oleh methemoglobin reduktase lain untuk mempertahankan besi hemoglobin dalam keadaan Fe2+ yang aktif secara fungsional. Pada salah satu kelainan eritrosit diturunkan yang sering ditemukan (yaitu defisiensi glukosa-6-fosfat dehidrogenase (G6PD)), eritrosit sangat rentan terhadap stres oksidasi (Hoffbrand et al, 2005)[14].
Faktor-faktor yang mempengaruhi fragilitas eritrosit
suntingAda 2 macam hemolisa, yaitu hemolisa osmotik dan hemolisa kimiawi. Hemolisa osmotik terjadi karena adanya perubahan yang besar antara tekanan osmosa cairan di dalam sel darah merah dengan cairan di sekeliling sel darah merah. Dalam hal ini tekanan osmosa sel darh merah jauh lebih besar daripada tekanan osmosa di luar sel. Tekanan osmosa di dalam sel darah merah sama dengan tekanan osmosa larutan NaCl 0.9%. Bila sel darah merah dimasukkan ke dalam larutan 0.8% belum terlihat adanya hemolisa, tetapi sel darah merah yang dimasukkan ke dalam larutan NaCl 0.4% hanya sebagian saja yang megalami hemolisa, sedangkan sebagian sel darah merah yang lainnya masih utuh. Perbedaan ini disebabkan karena umur sel darah merah, SDM yang sudah tua, membran selnya mudah pecah sedangkan SDM muda membran selnya masih kuat. Bila SDM dimasukkan ke dalam larutan NaCl 0.3% semua SDM akan mengalami hemolisa. Hal ini disebut hemolisa sempurna. Larutan yang mempunyai tekanan osmosa lebih kecil daripada tekanan osmosa ini SDM disebut larutan hipotonis, sedangkan larutan yang mempunyai tekanan osmosa lebih besar dari tekanan osmosa isi SDM disebut larutan hipertonis. Suatu larutan yang mempunyai tekanan osmosa yang sama besar dengan tekanan osmosa isi SDM disebut larutan isotonis. Sedangkan pada jenis hemolisa kimiawi, SDM dirusak oleh macam-macam substansi kimia. Dinding SDM terutama terdiri dari lipid dan protein, membentuk suatu lapisan lipoprotein. Jadi, setiap substansi kimia yang dapat melarutkan lemak (pelarut lemak) dapat merusak atau melarutkan membran SDM. Kita mengenal bermacam-macam pelarut lemak, yaitu kloroform, aseton, alkohol benzen, dan eter. Substansi lain yang dapat merusak membran SDM diantaranya adalah bisa ular, bisa kalajengking, garam empedu, saponin, nitrobenzen, pirogalol, asam karbon, resin, dan senyawa arsen. (Asscalbiass, 2011) Sel penyusun suatu organisme pasti berada dalam suatu cairan yang mengandung berbagai zat yang diperlukan oleh sel. Cairan tersebut berupa cairan ekstraseluler yang dapat dibedakan menjadi cairan interstitial dan/atau plasma darah. Sel pada umumnya berada dalam cairan interstitial, sedangkan eritrosit berada dalam plasma darah. Membran sel eritrosit seperti hanya membran sel lainnya tersusun atas lipid bilyer, dan bersifat semipermeabel. Pada kondisi cairan hipertonis, maka air akan berpindah dari dalam eritrosit ke luar sehingga eritrosit akan mengalami penyusutan (krenasi). Sebaliknya pada kondisi larutan hipotonis, maka air akan masuk ke dalam sitoplasma eritrosit sehingga eritrosit akan menggembung yang kemudian pecah (lisis). Kecepatan hemolisis dan krenasi eritrosit dipengaruhi oleh konsentrasi larutan (Syamsuri 2000).
Eritrosit pada manusia
suntingKepingan eritrosit manusia memiliki diameter sekitar 6-8 μm dan ketebalan 2 μm, lebih kecil daripada sel-sel lainnya yang terdapat pada tubuh manusia.[15] Eritrosit normal memiliki volume sekitar 9 fL (9 femtoliter) Sekitar sepertiga dari volume diisi oleh hemoglobin, total dari 270 juta molekul hemoglobin, di mana setiap molekul membawa 4 gugus heme.
Orang dewasa memiliki 2–3 × 1013 eritrosit setiap waktu (wanita memiliki 4-5 juta eritrosit per mikroliter darah dan pria memiliki 5-6 juta. Sedangkan orang yang tinggal di dataran tinggi yang memiliki kadar oksigen yang rendah maka cenderung untuk memiliki sel darah merah yang lebih banyak). Eritrosit terkandung di darah dalam jumlah yang tinggi dibandingkan dengan partikel darah yang lain, seperti misalnya sel darah putih yang hanya memiliki sekitar 4000-11000 sel darah putih dan platelet yang hanya memiliki 150000-400000 di setiap mikroliter dalam darah manusia.
Pada manusia, hemoglobin dalam sel darah merah mempunyai peran untuk mengantarkan lebih dari 98% oksigen ke seluruh tubuh, sedangkan sisanya terlarut dalam plasma darah.
Eritrosit dalam tubuh manusia menyimpan sekitar 2.5 gram besi, mewakili sekitar 65% kandungan besi di dalam tubuh manusia.[16][17]
Daur hidup
suntingProses di mana eritrosit diproduksi dinamakan eritropoiesis. Secara terus-menerus, eritrosit diproduksi di sumsum tulang merah, dengan laju produksi sekitar 2 juta eritrosit per detik (Pada embrio, hati berperan sebagai pusat produksi eritrosit utama). Produksi dapat distimulasi oleh hormon eritropoietin (EPO) yang disintesa oleh ginjal. Hormon ini sering digunakan dalam aktivitas olahraga sebagai doping. Saat sebelum dan sesudah meninggalkan sumsum tulang belakang, sel yang berkembang ini dinamai retikulosit dan jumlahnya sekitar 1% dari seluruh darah yang beredar.
Eritrosit dikembangkan dari sel punca melalui retikulosit untuk mendewasakan eritrosit dalam waktu sekitar 7 hari dan eritrosit dewasa —dengan sebuah percobaan untuk menandai eritrosit dengan besi radioaktif— terbukti akan hidup selama 120 hari.[18]
Polimorfisme dan kelainan
suntingMorfologi sel darah merah yang normal adalah bikonkaf. Cekungan (konkaf) pada eritrosit digunakan untuk memberikan ruang pada hemoglobin yang akan mengikat oksigen. Tetapi, polimorfisme yang mengakibatkan abnormalitas pada eritrosit dapat menyebabkan munculnya banyak penyakit. Umumnya, polimorfisme disebabkan oleh mutasi gen pengkode hemoglobin, gen pengkode protein transmembran, ataupun gen pengkode protein sitoskeleton. Polimorfisme yang mungkin terjadi antara lain adalah anemia sel sabit, Duffy negatif, Glucose-6-phosphatase deficiency (defisiensi G6PD), talasemia, kelainan glikoporin, dan South-East Asian Ovalocytosis (SAO).[19]
Catatan kaki
sunting- ^ a b "John W. Kimball's Biology pages - Blood". Diarsipkan dari versi asli tanggal 2009-10-08. Diakses tanggal 2010-02-14.
- ^ a b Laura Dean. Blood Groups and Red Cell Antigens
- ^ Maton, Anthea (1993). Human Biology and Health. Englewood Cliffs, New Jersey, USA: Prentice Hall. ISBN 0-13-981176-1.
- ^ SNYDER, GREGORY K. (1999-04-01). "Red Blood Cells: Centerpiece in the Evolution of the Vertebrate Circulatory System". American Zoologist. 39 (2): 189–198. doi:10.1093/icb/39.2.189.
- ^ Ruud, J. T. 1954. Vertebrates without erythrocytes and blood pigment. Nature 117:848-850.
- ^ Carroll, Sean (2006). The Making of the Fittest. W.W. Norton.
- ^ W. D. Cohen. The cytomorphic system of anucleate non-mammalian erythrocytes.[pranala nonaktif permanen] Protoplasma, vol 113 no 1, February 1982
- ^ (Inggris) "Maturational Loss of the Vitamin C Transporter in Erythrocytes". Department of Medicine, Vanderbilt University School of Medicine; James M. May, Zhi-chao Qu, Huan Qiao, dan Mark J. Koury. Diakses tanggal 2010-11-26.
- ^ Wan, Jiandi (2008-10-15). "Dynamics of shear-induced ATP release from red blood cells". Proceedings of the National Academy of Sciences of the United States of America. doi:0805779105 Periksa nilai
|doi=(bantuan). PMID 18922780. - ^ Diesen, Diana L (2008-08-29). "Hypoxic vasodilation by red blood cells: evidence for an s-nitrosothiol-based signal". Circulation Research. 103 (5): 545–53. doi:CIRCRESAHA.108.176867 Periksa nilai
|doi=(bantuan). PMID 18658051. - ^ Red blood cells do more than just carry oxygen. New findings by NUS team show they aggressively attack bacteria too., The Straits Times, 1 September 2007
- ^ Jiang N, Tan NS, Ho B, Ding JL. Respiratory protein-generated reactive oxygen species as an antimicrobial strategy. Nature Immunology, 26 August 2007. PMID 17721536.
- ^ Beveland, Gerrit; Rameley, Judith A. (1988). Dasar-dasar Histologi, Edisi Kedelapan. Terjemah oleh Wisnu Gunarso. Hlm.97 – 99. Jakarta: Penerbit Erlangga.
- ^ a b Hoffbrand, A Victor (2015-11-06). "Megaloblastic Anaemia". Postgraduate Haematology: 53–71. doi:10.1002/9781118853771.ch5.
- ^ Hillman, Robert S.; Ault, Kenneth A.; Rinder, Henry M. (2005), Hematology in Clinical Practice: A Guide to Diagnosis and Management (edisi ke-4), McGraw-Hill Professional, hlm. 1, ISBN 0071440356
- ^ Iron Metabolism, University of Virginia Pathology. Accessed 22 September 2007.
- ^ Iron Transport and Cellular Uptake by Kenneth R. Bridges, Information Center for Sickle Cell and Thalassemic Disorders. Accessed 22 September 2007.
- ^ Villee, Claude A.; Walker Jr., Warren F.; Barnes, Robert D. [1973]. Zoologi Umum: Edisi Keenam. 1:185. Alihbahasa oleh Nawangsari Sugiri, dan J. Sugiri. Jakarta: Penerbit Erlangga.
- ^ Kwiatkowski DP. 2005. How malaria has affected the human genome and what human genetic can teach us about malaria. Am. J. Hum. Genet. 77: 171-92.