Kurium(III) klorida
senyawa kimia
(Dialihkan dari Cl3Cm)
Kurium(III) klorida adalah sebuah senyawa anorganik dengan rumus CmCl3.
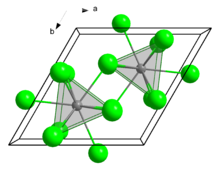 Struktur kristal
| |
| Penanda | |
|---|---|
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| |
| |
| Sifat | |
| Cl3Cm | |
| Massa molar | 353,35 g·mol−1 |
| Titik lebur | 695 °C (1.283 °F; 968 K)[butuh rujukan] |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Struktur
suntingKurium(III) klorida memiliki geometri prisma trigonal bertudung-tiga 9-koordinat.[1]
Sintesis
sunting- Reaksi gas hidrogen klorida dengan kurium dioksida, kurium(III) oksida, atau kurium(III) oksiklorida pada suhu 400-600 °C:
- CmOCl + 2HCl → CmCl
3 + H
2O
- CmOCl + 2HCl → CmCl
- Pelarutan logam kurium dalam asam klorida encer:[2]
- 2Cm + 6HCl → 2CmCl
3 + 3H
2
- 2Cm + 6HCl → 2CmCl
Metode ini memiliki sejumlah kelemahan yang terkait dengan proses hidrolisis dan hidrasi yang sedang berlangsung dari senyawa yang dihasilkan dalam larutan berair. Oleh karena itu, sulit untuk mendapatkan kurium(III) klorida murni dengan menggunakan reaksi ini.
Pembuatan
suntingKurium(III) klorida dapat dibuat melalui reaksi antara kurium nitrida dengan kadmium klorida.[3]
Referensi
sunting- ^ Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (edisi ke-2). Butterworth, Britania Raya. hlm. 1270.
- ^ Wallmann, J. C.; Fuger, J.; Peterson, J. R.; Green, J. L. (1 November 1967). "Crystal structure and lattice parameters of curium trichloride". Journal of Inorganic and Nuclear Chemistry (dalam bahasa Inggris). 29 (11): 2745–2751. doi:10.1016/0022-1902(67)80013-7. ISSN 0022-1902. Diakses tanggal 10 Februari 2024.
- ^ Hayashi, Hirokazu; Takano, Masahide; Otobe, Haruyoshi; Koyama, Tadafumi (Juli 2013). "Syntheses and thermal analyses of curium trichloride". Journal of Radioanalytical and Nuclear Chemistry. 297 (1): 139–144. doi:10.1007/s10967-012-2413-7.