Asiklovir
Asiklovir (Acyclovir disingkat ACV) merupakan salah satu obat antivirus.[3] Obat ini digunakan terutama untuk pengobatan infeksi virus herpes simpleks, cacar air, dan herpes zoster. Penggunaan lainnya untuk pencegahan infeksi sitomegalovirus setelah transplantasi dan infeksi karena virus Epstein-Barr. Asiklovir tersedia dalam bentuk tablet, injeksi intravena, dan krim.[4]
| |
|---|---|

| |
| Nama sistematis (IUPAC) | |
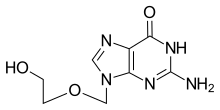
| 2-Amino-1,9-dihydro-9-((2-hydroxyethoxy)methyl)-6H-purin-6-one | |
| Data klinis | |
| Nama dagang | Acifar, Matrovir, Zovirax, lainnya[1] |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a681045 |
| Data lisensi | US FDA:link |
| Kat. kehamilan | B3(AU) B(US) |
| Status hukum | Harus dengan resep dokter (S4) (AU) ℞-only (CA) POM (UK) ℞-only (US) |
| Rute | Intravena, peroral, topikal (termasuk salep mata) |
| Data farmakokinetik | |
| Bioavailabilitas | 15–20% (oral)[2] |
| Ikatan protein | 9–33%[2] |
| Metabolisme | Hepatik |
| Waktu paruh | 2–4 jam |
| Ekskresi | Renal (62–90% dalam bentuk senyawa utuh) |
| Pengenal | |
| Nomor CAS | 59277-89-3 |
| Kode ATC | J05AB01 D06BB03 S01AD03 |
| PubChem | CID 2022 |
| Ligan IUPHAR | 4829 |
| DrugBank | DB00787 |
| ChemSpider | 1945 |
| UNII | X4HES1O11F |
| KEGG | D00222 |
| ChEBI | CHEBI:2453 |
| ChEMBL | CHEMBL184 |
| Sinonim | asikloguanosin |
| Data kimia | |
| Rumus | C8H11N5O3 |
| SMILES | eMolecules & PubChem |
| |
| Data fisik | |
| Titik lebur | 256.5 °C (494 °F) |
Efek samping yang umum terjadi antara lain mual dan diare. Potensi efek samping yang serius antara lain masalah ginjal dan trombositopenia. Obat ini perlu diberikan perhatian khusus jika pasien mempunyai fungsi ginjal dan hati yang buruk.[4] Obat ini dianggap aman untuk digunakan selama masa kehamilan.[4][5] Dan aman digunakan selama menyusui.[6][7] Asiklovir merupakan analog asam nukleat yang terbuat dari guanosin. Kerja dari obat ini untuk menurunkan produksi DNA virus.[4]
Asiklovir ditemukan pada tahun 1977.[8] Obat ini termasuk daftar obat penting yang diperlukan dalam sistem kesehatan dasar menurut WHO.[9] Obat ini tersedia dalam bentuk obat generik dan dijual di bawah harga obat bermerek di seluruh dunia.[1] Kisaran harga dari tahun 2014-2016 antara US$0,03 (Rp300,-) dan US$0,12 (Rp1.200,-) per tablet.[10][11] Biaya pengobatan dengan obat ini hingga sembuh di Amerika Serikat kurang dari US$25.[6]
Kegunaan medis
suntingAsiklovir digunakan untuk mengobati infeksi virus herpes simpleks dan virus varicella zoster, termasuk:[2][12][13]
- Herpes simpleks genital (pengobatan dan pencegahan)
- Herpes simpleks neonatus (bayi baru melahirkan)
- Herpes simpleks labialis
- Herpes zoster
- Cacar air pada pasien imunokompromais
- Herpes simpleks ensefalitis
- Infeksi HSV mukokutan akut pada pasien imunokompromais
- Herpes simpleks keratitis (pada mata) dan herpes simpleks blefaritis (bentuk kronis dari infeksi herpes mata)
- Pencegahan dari virus herpes pada pasien imunokompromais (seperti pasien yang menjalani kemoterapi kanker)[14]
Tetapi asiklovir peroral, tidak menunjukan penurunan risiko rasa nyeri pada herpes zoster.[15] Pada pasien herpes di mata, asiklovir ditemukan lebih efektif daripada idoksuridin atau vidarabin dengan membandingkan tingkat keberhasilan mata yang dapat disembuhkan[butuh pemutakhiran]
Asiklovir intravena efektif untuk mengobati penyakit yang parah yang disebabkan oleh spesies yang berbeda dari famili herpesviridae, termasuk infeksi lokal parah dari virus herpes, herpes genital parah, cacar air, dan herpes ensefalitis. Obat ini juga efektif mengobati infeksi herpes sistemik, eksem yang disebabkan herpes dan meningitis yang disebabkan herpes simpleks. Tinjauan penelitian dari tahun 1980-an menunjukkan adanya efek dalam mengurangi jumlah dan durasi lesi herpes jika asiklovir diberikan di tahap awal infeksi.[16] Penelitian terbaru menunjukkan efektivitas dari asiklovir topikal untuk mengurangi jumlah lesi pada infeksi tahap awal dan akhir.[17] Dari hasil percobaan, asiklovir tidak memiliki efek dalam mencegah transmisi HIV, tetapi dapat membantu memperlambat perkembangan HIV pada pasien yang tidak mengonsumsi obat antiretroviral (ART). Hasil temuan ini menekankan pentingnya pengujian obat non-ART yang sederhana dan murah, seperti asiklovir dan kotrimoksazol, pada pasien HIV.[18]
Kehamilan
suntingAsiklovir diklasifikasikan sebagai obat Kategori B,[19] CDC telah menyatakan bahwa asiklovir dapat digunakan pada herpes genitali rekuren.[20] Untuk infeksi HSV yang parah, asiklovir intravena dapat digunakan.[21] Studi pada mencit, kelinci, dan tikus (dengan dosis setara dengan 10 kali lebih tinggi dari yang digunakan pada manusia) yang diberikan selama organogenesis gagal menunjukkan adanya kecacatan pada bayi hewan tersebut.[22] Penelitian pada tikus yang diberikan dosis setara dengan 63 kali lebih tinggi dari dosis manusia[Note 1] pada 10 hari gestasi menunjukkan adanya anomali pada kepala dan ekor.[22]
Asiklovir direkomendasikan oleh CDC untuk pengobatan Varicella selama kehamilan, terutama selama trimester kedua dan ketiga[21]
Asiklovir diekskresikan di ASI, oleh karena itu dianjurkan untuk berhati-hati ketika digunakan pada wanita yang sedang menyusui. Dalam studi pengujian yang terbatas menunjukkan bayi yang menyusui terpapar kira-kira 0,3 mg/kg/hari setelah pemberian asiklovir oral pada ibu. Jika ibu memiliki lesi herpes di dekat atau di payudara, menyusui harus dihindari.[19][23]
Efek yang tidak diinginkan
suntingTerapi sistemik
suntingEfek obat yang tidak diinginkan umumnya (≥1% dari pasien) berkaitan dengan terapi asiklovir sistemik (peroral atau intravena) termasuk: mual, muntah, diare, encefalopaty (hanya pada penggunaan intravena), reaksi pada tempat injeksi (hanya pada penggunaan intravena) dan sakit kepala. Dalam dosis tinggi, halusinasi mungkin terjadi. Efek yang tidak diinginkan yang jarang (0.1–1% dari pasien) antara lain: vertigo, kebingungan, pusing, edema, arthralgia, sakit tenggorokan, sembelit, sakit perut, hilang rambut, ruam dan lemah. Efek yang tidak diinginkan yang langka (<0.1% dari pasien) antara lain: koma, kejang, neutropenia, leukopenia, kristaluria, anoreksia, kelelahan, hepatitis, sindrom Stevens–Johnson, toxic epidermal necrolysis, thrombotic thrombocytopenic purpura dan anaphylaxis.[12]
Asiklovir intravena juga dapat menyebabkan nefrotoksisitas reversibel hingga 5%-10% dari pasien karena pengendapan kristal asiklovir di ginjal, efek ini dapat berakhir dengan penghentian pemberian asiklovir. Nefropati yang disebabkan kristal asiklovir lebih umum terjadi ketika asiklovir diberikan secara infusa cepat dan pada pasien dengan dehidrasi atau gangguan ginjal. Hidrasi yang cukup, kecepatan infus lebih rendah, dan pemberian dosis sesuai fungsi renal dapat mengurangi risiko ini.[24][25][26]
Terapi Topikal
suntingKrim asiklovir dapat menyebabkan (≥1% dari pasien) kulit mengering atau sensasi terbakar di kulit. Efek yang tidak diinginkan yang jarang antara lain eritema atau gatal-gatal.[12] Ketika diberikan di mata, asiklovir menyebabkan (≥1% dari pasien) sensasi menyengat di mata. Terkadang asiklovir oftalmik menyebabkan (0.1–1% dari pasien), superficial punctate keratitis atau reaksi alergi.[12]
Interaksi obat
sunting- Ketokonazol: Studi in-vitro menunjukkan jika asiklovir dan ketokonazol diberikan secara bersamaan akan meningkatkan aktivitas antivirus terhadap HSV-1 dan HSV-2 (efek sinergis). Namun, efek ini belum dibuktikan secara klinis (studi in-vivo) dan perlu lebih banyak penelitian yang dilakukan untuk mengetahui potensi sesungguhnya dari efek ini.[27]
- Probenesid: hasil penelitian menunjukkan jika probenesid diberikan bersamaan dengan asiklovir maka waktu paruh dari asiklovir akan meningkat, serta terjadi penurunan ekskresi melalui urin, dan klirens renaln juga menurun.[19]
- Interferon: akan memberikan efek sinergis bila diberikan dengan asiklovir secara bersamaan dan perlu pemantauan khusus ketika memberikan asiklovir kepada pasien yang menerima interferon intravena.[28]
- Zidovudin: Meskipun sering diberikan dengan asiklovir pada pasien HIV, telah dilaporkan terjadi efek neurotoksisitas pada setidaknya satu pasien yang juga mengalami rasa kantuk berat dan lemas selama 30-60 hari setelah menerima asiklovir intravena; gejala tersebut berhenti ketika penggunaan asiklovir dihentikan.[29]
Deteksi dalam cairan biologis
suntingKadar asiklovir dapat dihitung di plasma atau serum untuk memantau akumulasi obat pada pasien dengan gangguan ginjal atau untuk mengonfirmasi hasil diagnosis pasien yang diduga mengalami overdosis obat.[30]
Mekanisme aksi obat
suntingAsiklovir diubah oleh timidin kinase dari virus menjadi asiklovir monofosfat, yang kemudian diubah oleh enzim kinase dari inang menjadi asiklovir trifosfat (ACV-TP).[22] ACV-TP menghambat secara kompetitif dan menginaktivasi DNA polimerase HSV yang akhirnya mencegah sintesis DNA virus tanpa mempengaruhi proses sintesis pada sel normal (pasien).[22][31][32]
Resistensi
suntingResistensi asiklovir jarang terjadi pada orang dengan sistem imun tubuh yang normal, tapi lebih umum terjadi (sampai 10%) pada orang-orang dengan immunodefisiensi (seperti penerima transplantasi organ dan pasien AIDS akibat infeksi HIV). Mekanisme terjadinya resistensi pada HSV antara lain kurangnya timidin kinase virus; dan mutasi pada timidin kinase virus atau DNA polymerase, yang mengubah sensitivitas substrat.[33][34]
Mikrobiologi
suntingAsiklovir efektif untuk melawan sebagian besar spesies virus dari famili herpesviridae. Aktivitas asiklovir semakin menurun sesuai urutan:[35][36]
- Virus herpes simpleks tipe I (HSV-1) – paling aktif
- Virus herpes simpleks tipe II (HSV-2)
- Virus varicella zoster (VZV)
- Virus Epstein-Barr (EBV)
- Sitomegalovirus (CMV) – paling tidak aktif
Farmakokinetika
suntingAsiklovir tidak larut di air dan mempunyai bioavailabilitas oral yang buruk (15–30%), sehingga pemberian secara intravena diperlukan jika asiklovir dibutuhkan dengan konsentrasi yang tinggi dalam plasma. Ketika diberikan secara peroral, puncak konsentrasi di plasma tercapai setelah 1–2 jam pemberian. Asiklovir terdistribusi dengan baik di tubuh; pengikatan protein sekitar 9 sampai 33%.[37] Waktu paruh (waktu yang diperlukan agar konsentrasi obat dalam plasma berkurang menjadi setengahnya, t1/2) asiklovir tergantung umur pasien; neonatus (bayi yang baru lahir) mempunyai waktu t1/2 selama 4 jam, anak 1–12 tahun waktu t1/2 selama 2–3 jam, dan dewasa waktu t1/2 selama 3 jam.[2]
Sejarah
suntingAsiklovir dipandang sebagai awal dari era baru dalam terapi antivirus, asiklovir sangat selektif dengan sitotoksisitas yang rendah.[3] Sejak penemuannya di pertengahan 1970-an, obat ini digunakan untuk pengobatan infeksi yang disebabkan oleh famili virus Herpes termasuk virus Herpes zoster dan Varicella zoster. Nukleosida yang diisolasi dari spons Karibia, Cryptotethya crypta, menjadi dasar untuk sintesis dari asiklovir.[38][39][40] Asiklovir ditemukan oleh Howard Schaffer setelah penelitiannya dengan Robert Vince, S. Bittner dan S. Gurwara mengenai analog adenosin asikloadenosin yang menunjukkan aktivitas antivirus.[41] Kemudian, Schaffer bergabung dengan Burroughs Wellcome dan melanjutkan pengembangan asiklovir dengan ahli farmakologi Gertrude B. Elion.[42] Paten asiklovis di Amerika Serkat diterbitkan pada tahun 1979.[43]
Vince kemudian menemukan abacavir, sebuah obat nRTI untuk pasien HIV.[44]
Penamaan dan Harga
suntingPenamaan
suntingAciclovir adalah nama menurut INN dan BAN sementara acyclovir adalah nama menurut USAN. Di Indonesia nama resmi obat ini adalah asiklovir
Awalnya dipasarkan dengan nama dagang Zovirax; paten obat berakhir pada tahun 1990-an dan sejak saat itu menjadi obat generik dan dijual dengan berbagai merek di seluruh dunia.[1]
Harga
suntingHarga per tablet 400 mg di bulan Maret 2016 antara US$0,03 (Rp300,-) sampai US$0,12 (Rp1.200,-).[10][11]
Catatan
sunting- ^ Subject to the same conditions as before
Referensi
sunting- ^ a b c "Aciclovir". Drugs.com. Diakses tanggal 6 September 2015.
- ^ a b c d "Zovirax (acyclovir) dosing, indications, interactions, adverse effects, and more". Medscape Reference. WebMD. Diakses tanggal 5 February 2014.
- ^ a b de Clercq, Erik; Field, Hugh J (5 October 2005). "Antiviral prodrugs – the development of successful prodrug strategies for antiviral chemotherapy". British Journal of Pharmacology. 147 (1). Wiley-Blackwell (dipublikasikan tanggal January 2006). hlm. 1–11. doi:10.1038/sj.bjp.0706446. PMC 1615839 . PMID 16284630.
- ^ a b c d "Acyclovir". The American Society of Health-System Pharmacists. Diakses tanggal Jan 1, 2015.
- ^ "Prescribing medicines in pregnancy database". Australian Government. 3 March 2014. Diakses tanggal 22 April 2014.
- ^ a b Hamilton, Richart (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. hlm. 59. ISBN 9781284057560.
- ^ "Acyclovir use while Breastfeeding". Mar 10, 2015. Diakses tanggal 8 March 2016.
Even with the highest maternal dosages, the dosage of acyclovir in milk is only about 1% of a typical infant dosage and would not be expected to cause any adverse effects in breastfed infants
- ^ Clercq, edited by Erik De (2013). Anti-viral agents (edisi ke-1). San Diego, CA: Academic Press. hlm. 5. ISBN 9780124055377.
- ^ "WHO Model List of Essential Medicines" (PDF). World Health Organization. October 2013. Diakses tanggal 22 April 2014.
- ^ a b "Aciclovir". International Drug Price Indicator Guide. Diarsipkan dari versi asli tanggal 2017-03-05. Diakses tanggal 6 September 2015.
- ^ a b "Pharmacy Pricing". Medicaid. March 2016. Diarsipkan dari versi asli tanggal 2016-03-24. Diakses tanggal 8 March 2016.
- ^ a b c d Rossi, S, ed. (2013). Australian Medicines Handbook (edisi ke-2013). Adelaide: The Australian Medicines Handbook Unit Trust. ISBN 978-0-9805790-9-3.
- ^ Joint Formulary Committee (2013). British National Formulary (BNF) (edisi ke-65). London, UK: Pharmaceutical Press. ISBN 978-0-85711-084-8.
- ^ Elad S, Zadik Y, Hewson I, et al. (August 2010). "A systematic review of viral infections associated with oral involvement in cancer patients: a spotlight on Herpesviridea". Support Care Cancer. 18 (8): 993–1006. doi:10.1007/s00520-010-0900-3. PMID 20544224.
- ^ Chen, N; Li, Q; Yang, J; Zhou, M; Zhou, D; He, L (Feb 6, 2014). "Antiviral treatment for preventing postherpetic neuralgia". The Cochrane database of systematic reviews. 2: CD006866. doi:10.1002/14651858.CD006866.pub3. PMID 24500927.
- ^ Graham Worrall (6 Jan 1996). "Acyclovir in recurrent herpes labialis". BMJ. 312 (7022): 6. doi:10.1136/bmj.312.7022.6. PMC 2349724 . PMID 8555890.
- ^ "Acyclovir cream for treatment of herpes simplex labialis: results of two randomized, double-blind, vehicle-controlled, multicenter clinical trials". Antimicrob. Agents Chemother. 46: 2238–43. 2002. doi:10.1128/aac.46.7.2238-2243.2002. PMC 127288 . PMID 12069980.
- ^ Mascolinli, M; Kort, R (June 2010). "5th International AIDS Society Conference on HIV Pathogenesis, Treatment and Prevention: summary of key research and implications for policy and practice - biomedical prevention" (PDF). Journal of the International AIDS Society. 13 Suppl 1 (Suppl 1): S4. doi:10.1186/1758-2652-13-S1-S4. PMC 2880255 . PMID 20519025.
- ^ a b c FDA and GSK.
- ^ "Drugs for non-HIV viral infections". Treatment guidelines from the Medical Letter. 3 (32): 23–32. 2005. PMID 15767977.
- ^ a b Centers for Disease Control and Prevention.
- ^ a b c d "PRODUCT INFORMATION NAME OF THE DRUG OZVIR TABLETS" (PDF). TGA eBusiness Services. Ranbaxy Australia Pty Ltd. 26 August 2011. Diakses tanggal 6 February 2014.
- ^ Gartner LM, Morton J, Lawrence RA, et al, "Breastfeeding and the Use of Human Milk," Pediatrics, 2005, 115(2):496-506
- ^ Razonable, RR (October 2011). "Antiviral drugs for viruses other than human immunodeficiency virus" (PDF). Mayo Clinic proceedings. Mayo Clinic. 86 (10): 1009–26. doi:10.4065/mcp.2011.0309. PMC 3184032 . PMID 21964179.
- ^ Brigden D, Rosling AE, Woods NC (July 1982). "Renal function after acyclovir intravenous injection". The American Journal of Medicine. 73 (1A): 182–5. doi:10.1016/0002-9343(82)90087-0. PMID 6285711.
- ^ Sawyer MH, Webb DE, Balow JE, Straus SE (June 1988). "Acyclovir-induced renal failure. Clinical course and histology". The American Journal of Medicine. 84 (6): 1067–71. doi:10.1016/0002-9343(88)90313-0. PMID 3376977.
- ^ Pottage Jr, J. C.; Kessler, H. A.; Goodrich, J. M.; Chase, R; Benson, C. A.; Kapell, K; Levin, S (1986). "In vitro activity of ketoconazole against herpes simplex virus". Antimicrobial Agents and Chemotherapy. 30 (2): 215–9. doi:10.1128/aac.30.2.215. PMC 180521 . PMID 3021048.
- ^ GlaxoSmithKline.
- ^ Bach, M. C. (1987). "Possible drug interaction during therapy with azidothymidine and acyclovir for AIDS". New England Journal of Medicine. 316 (9): 547–548. doi:10.1056/NEJM198702263160912. PMID 3468354.
- ^ Baselt, RC (2008). Disposition of toxic drugs and chemicals in man (edisi ke-8th). Foster City, CA: Biomedical Publications. hlm. 29–31. ISBN 9780962652370.
- ^ "Acyclovir (acyclovir) Capsule Acyclovir (acyclovir) Tablet [Genpharm Inc.]". DailyMed. Genpharm Inc. November 2006. Diakses tanggal 5 February 2014.
- ^ "Aciclovir Tablets BP 400mg - Summary of Product Characteristics (SPC)". electronic Medicines Compendium. Actavis UK Ltd. 20 August 2012. Diarsipkan dari versi asli tanggal 2014-02-22. Diakses tanggal 5 February 2014.
- ^ Sweetman, S, ed. (7 August 2013). "Aciclovir". Martindale: The Complete Drug Reference. London, UK: Pharmaceutical Press. Diakses tanggal 6 February 2014.
- ^ Piret J, Boivin G (2011). "Resistance of herpes simplex viruses to nucleoside analogues: mechanisms, prevalence, and management". Antimicrob. Agents Chemother. 55 (2): 459–72. doi:10.1128/AAC.00615-10. PMC 3028810 . PMID 21078929.
- ^ O'Brien, JJ; Campoli-Richards, DM (1989). "Acyclovir. An updated review of its antiviral activity, pharmacokinetic properties and therapeutic efficacy". Drugs. 37 (3): 233–309. doi:10.2165/00003495-198937030-00002. PMID 2653790.
- ^ Wagstaff, AJ; Faulds, D; Goa, KL (January 1994). "Aciclovir. A reappraisal of its antiviral activity, pharmacokinetic properties and therapeutic efficacy". Drugs. 47 (1): 153–205. doi:10.2165/00003495-199447010-00009. PMID 7510619.
- ^ Aciclovir Tablets BP 400mg - Summary of Product Characteristics (SPC) - (eMC)
- ^ Garrison, Tom (1999). Oceanography: An Invitation to Marine Science, 3rd ed. Belmont, CA: Wadsworth Publishing Company. hlm. 471.
- ^ Sepčić, K. (2000). "Bioactive Alkylpyridinium Compounds from Marine Sponges". Toxin Reviews. 19 (2): 139–160. doi:10.1081/TXR-100100318.
- ^ Laport, M. S.; Santos, O. C.; Muricy, G (2009). "Marine sponges: Potential sources of new antimicrobial drugs". Current pharmaceutical biotechnology. 10 (1): 86–105. doi:10.2174/138920109787048625. PMID 19149592.
- ^ Schaffer, Howard; Robert Vince; S. Bittner; S. Gurwara (1971). "Novel substrate of adenosine deaminase". Journal of Medicinal Chemistry. 14 (4): 367–369. doi:10.1021/jm00286a024. PMID 5553754.
- ^ Elion, Gertrude; Furman PA; Fyfe, James A.; De Miranda, Paulo; Beauchamp, Lilia; Schaeffer, Howard J. (1977). "Selectivity of action of an antiherpetic agent, 9-(2-hydroxyethoxymethyl)guanine". Proc Natl Acad Sci USA. 74 (12): 5716–5720. Bibcode:1977PNAS...74.5716E. doi:10.1073/pnas.74.12.5716. PMC 431864 . PMID 202961.
- ^ US 4146715
- ^ Vince R (2008). "A brief history of the development of Ziagen". Chemtracts. 21: 127–134.
Bacaan lebih lanjut
sunting- Hazra, S; Konrad, M; Lavie, A (2010). "The sugar ring of the nucleoside is required for productive substrate positioning in the active site of human deoxycytidine kinase (dCK): Implications for the development of dCK-activated acyclic guanine analogues". Journal of Medicinal Chemistry. 53 (15): 5792–800. doi:10.1021/jm1005379. PMC 2936711 . PMID 20684612.
- Harvey Stewart C. in Remington’s Pharmaceutical Sciences 18th edition: (ed. Gennard, Alfonso R.) Mack Publishing Company, 1990. ISBN 0-912734-04-3.
- Huovinen P., Valtonen V. in Kliininen Farmakologia (ed. Neuvonen et al.). Kandidaattikustannus Oy, 1994. ISBN 951-8951-09-8.
- Périgaud C.; Gosselin G.; Imbach J.-L. (1992). "Nucleoside analogues as chemotherapeutic agents: a review". Nucleosides and nucleotides. 11 (2–4).
- Rang H.P., Dale M.M., Ritter J.M.: Pharmacology, 3rd edition. Pearson Professional Ltd, 1995. 2003 (5th) edition ISBN 0-443-07145-4; 2001 (4th) edition ISBN 0-443-06574-8; 1990 edition ISBN 0-443-03407-9.